
| 2��9+2-8 |
| 2 |
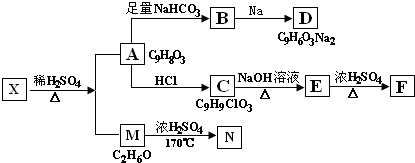
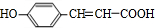 ��X��Ũ���ᡢ��������������A��M��M�ķ���ʽΪC2H6O��MΪ�Ҵ����Ҵ�������ȥ��Ӧ������ϩ��NΪ��ϩ��XΪ
��X��Ũ���ᡢ��������������A��M��M�ķ���ʽΪC2H6O��MΪ�Ҵ����Ҵ�������ȥ��Ӧ������ϩ��NΪ��ϩ��XΪ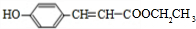 ��A��̼�����Ʒ�Ӧ����B��Ϊ
��A��̼�����Ʒ�Ӧ����B��Ϊ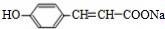 ��B��Na��Ӧ����D��DΪ
��B��Na��Ӧ����D��DΪ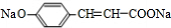 ��A��HCl��Ӧ����C��C�ķ���ʽΪC9H9ClO3����A��C�ķ���ʽ��֪�������ӳɷ�Ӧ��C����������ˮ��Һ�з���ˮ�ⷴӦ����E��E��Ũ���ᡢ���ȵ�����������F��F�����г���2�������⣬����һ����Ԫ����Ӧ����������Ӧ����CΪ
��A��HCl��Ӧ����C��C�ķ���ʽΪC9H9ClO3����A��C�ķ���ʽ��֪�������ӳɷ�Ӧ��C����������ˮ��Һ�з���ˮ�ⷴӦ����E��E��Ũ���ᡢ���ȵ�����������F��F�����г���2�������⣬����һ����Ԫ����Ӧ����������Ӧ����CΪ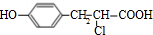 ��EΪ
��EΪ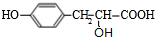 ��FΪ
��FΪ ���ݴ˽��
���ݴ˽��| 2��9+2-8 |
| 2 |
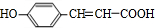 ��
��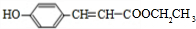 ��A��̼�����Ʒ�Ӧ����B��Ϊ
��A��̼�����Ʒ�Ӧ����B��Ϊ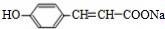 ��B��Na��Ӧ����D��DΪ
��B��Na��Ӧ����D��DΪ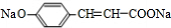 ��A��HCl��Ӧ����C��C�ķ���ʽΪC9H9ClO3����A��C�ķ���ʽ��֪�������ӳɷ�Ӧ��C����������ˮ��Һ�з���ˮ�ⷴӦ����E��E��Ũ���ᡢ���ȵ�����������F��F�����г���2�������⣬����һ����Ԫ����Ӧ����������Ӧ����CΪ
��A��HCl��Ӧ����C��C�ķ���ʽΪC9H9ClO3����A��C�ķ���ʽ��֪�������ӳɷ�Ӧ��C����������ˮ��Һ�з���ˮ�ⷴӦ����E��E��Ũ���ᡢ���ȵ�����������F��F�����г���2�������⣬����һ����Ԫ����Ӧ����������Ӧ����CΪ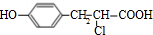 ��EΪ
��EΪ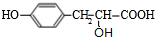 ��FΪ
��FΪ ��
��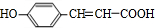 �������к��й����ţ����ǻ���̼̼˫�����Ȼ����������������У����ǻ����Ȼ���
�������к��й����ţ����ǻ���̼̼˫�����Ȼ����������������У����ǻ����Ȼ���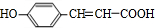 +NaHCO3��
+NaHCO3��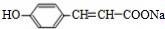 +H2O+CO2��
+H2O+CO2��| Ũ���� |
| 170�� |
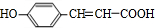 +NaHCO3��
+NaHCO3��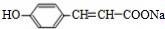 +H2O+CO2����
+H2O+CO2����| Ũ���� |
| 170�� |
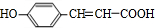 ��HCl�����ӳɷ�Ӧ����
��HCl�����ӳɷ�Ӧ����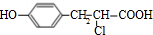 ��
��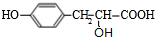 ����������Ӧ����
����������Ӧ���� ��
��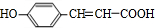 ���巢����Ӧʱ�������ǻ�����λ���Է���ȡ����Ӧ��C=C˫����Ӧ�ӳɷ�Ӧ����1molA���Ժ�3mol Br2��Ӧ��
���巢����Ӧʱ�������ǻ�����λ���Է���ȡ����Ӧ��C=C˫����Ӧ�ӳɷ�Ӧ����1molA���Ժ�3mol Br2��Ӧ��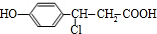 ��C1��NaOHˮ��Һ�з�Ӧ�Ļ�ѧ����ʽΪ
��C1��NaOHˮ��Һ�з�Ӧ�Ļ�ѧ����ʽΪ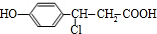 +3NaOH
+3NaOH| ˮ |
| �� |
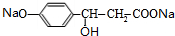 +NaCl+2H2O��
+NaCl+2H2O��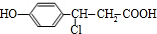 +3NaOH
+3NaOH| ˮ |
| �� |
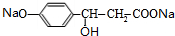 +NaCl+2H2O��
+NaCl+2H2O��


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��Fe3+��Na+��SO
| ||
B��H+��Fe2+��CI-��NO
| ||
C��Ag+��Na+��CO
| ||
D��AI3+��K+��CI-��AIO
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��Ba��OH��2��NaHSO4��Ba2++OH-+H++SO42-�TBaSO4��+H2O |
| B��Ba��OH��2��NaHSO4��Ba2++2OH-+2H++SO42-�TBaSO4��+2H2O |
| C��Ba��OH��2��KAl��SO4��2��2Ba2++4OH-+Al3++2SO42-�T2BaSO4��+AlO2- |
| D��Ba��OH��2��KAl��SO4��2��3Ba2++6OH-+2Al3++3SO42-�T3BaSO4��+2Al��OH��3�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��7.45g NaClO���6.02��1022��NaClO���� |
| B��1.00molNaClO������ClO-�ĵ�������Ϊ26��6.02��1023 |
| C��1 L 2 mol/L������ˮ��ɵõ�������������������ĿΪ2��6.02��1023 |
| D����2.00mol������ȫ����1.00 Lˮ�У��õ���Һ�����ʵ���Ũ��Ϊ2 mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��4.6g���ΪC2H6O���л������C-H����Ŀһ��Ϊ0.6NA | ||||
| B��8.7gMnO2��40mL 10mol/L��Ũ�����ַ�Ӧ�����ɵ�����������Ϊ0.1NA | ||||
| C��0.1molN2��0.3molH2���ܱ������У��ڴ��������³�ַ�Ӧ�����ɰ�������Ϊ0.2NA | ||||
D���ڷ�Ӧ5NH4NO3
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CaO |
| B��CuSO4��5H2O |
| C��NaOH |
| D��Na2O2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com