
下列有关中和热的说法正确的是( )
A.中和热的热化学方程式:H+(l)+OH-(l)===H2O(l)ΔH=-57.3 kJ/mol
B.准确测量中和热的实验过程中,至少需测定温度4次
C.环形玻璃搅拌棒材料若用铜代替,则测量出的中和热数值偏小
D.若稀酸溶液中H+与稀碱溶液中OH-的物质的量相等,则所测中和热数值更准确
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
火箭发射的燃料有很多,偏二甲肼(C2H8N2)是一种高能燃料,燃烧产生巨大能量,可作为航天运载火箭的推动力.下列叙述中正确的是( )
A. 6.02×1023个偏二甲肼分子的质量为60g
B. 偏二甲肼的摩尔质量为60g
C. 1mol偏二甲肼的质量为60g/mol
D. 6g偏二甲肼含有NA个偏二甲肼分子
查看答案和解析>>
科目:高中化学 来源: 题型:
在2L的密闭容器内,800℃时反应2NO(g)+O2(g)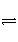
 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
(1) 写出该反应的平衡常数表达式:K=_____________________________________。
已知:K300℃>K350℃,则该反应是______热反应。
(2)下图表示NO2的变化的曲线是__________。用O2表示从0~2s内该反应的平均速率v=_____________________________________
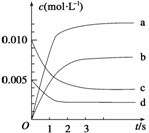
(3)能说明该反应已达到平衡状态的是________。
a.v(NO2)=2v(O2)
b.容器内压强保持不变
c.v逆(NO)=2v正(O2)
d.容器内密度保持不变
(4)为使该反应的反应速率增大,且平衡向正反应方向移动的是________。
a.及时分离出NO2气体b.适当升高温度c.增大O2的浓度d.选择高效催化剂
附加题:
查看答案和解析>>
科目:高中化学 来源: 题型:
根据下列三个反应的化学方程式:I2+SO2+2H2O═H2SO4+2HI;2FeCl2+Cl2═2FeCl3,2FeCl3+2HI═2FeCl2+2HCl+I2有关物质的还原性依次增强的顺序是( )
‚
|
| A. | I﹣>Fe2+>Cl﹣>SO2 | B. | Cl﹣>Fe2+>SO2>I﹣ |
|
| C. | Fe2+>I﹣>Cl﹣>SO2 | D. | SO2>I﹣>Fe2+>Cl﹣ |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)现有下列状态的物质①干冰 ②NaCl晶体 ③氨水 ④醋酸 ⑤酒精水溶液 ⑥铜 ⑦熔融的KOH ⑧蔗糖,其中属于电解质的是 (填序号),属于非电解质的是 (填序号),能导电的是 (填序号).
(2)某有色电解质溶液中,可能大量存在有Ag+、H+、Cu2+、OH﹣、Cl﹣等离子,你认为:一定有的离子是 ,一定没有的离子是 ,不能确定的离子 .
查看答案和解析>>
科目:高中化学 来源: 题型:
已知31 g白磷变成红磷放出18.39 kJ热量,下列两反应中:
P4(s)+5O2(g)===2P2O5(s) ΔH=Q1 kJ·mol-1
4P(红,s)+5O2(g)===2P2O5(s) ΔH=Q2kJ·mol-1
则下列说法中正确的是( )
A.Q1>Q2,白磷比红磷稳定 B.Q1>Q2,红磷比白磷稳定
C.Q1<Q2,白磷比红磷稳定 D.Q1<Q2,红磷比白磷稳定
查看答案和解析>>
科目:高中化学 来源: 题型:
对可逆反应2A(s)+3B(g)C(g)+2 D(g) ΔH<0,在一定条件下达到平衡,下列有关叙述正确的是( )
①增加A的量,平衡向正反应方向移动
②升高温度,平衡向逆反应方向移动,v (正)减小
③压强增大一倍,平衡不移动,v(正)、v(逆)不变
④增大B的浓度,v(正)>v(逆)
⑤加入催化剂,B的转化率提高
A.①② B.④ C.③ D.④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组顺序的排列不正确的是( )
A. 碱性强弱:NaOH>Mg(OH)2>Al(OH)3
B. 热稳定性:HF>HCl>H2S>PH3
C. 微粒半径:Na+>Mg2+>Al3+>F﹣
D. 熔点:SiO2>NaCl>I2>CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
下列电离方程式错误的是( )
A.CaCl2=Ca2++2Cl﹣ B.Na2SO4=2Na++SO42﹣
C.HNO3=H++NO3﹣ D.KClO3=K++Cl﹣+3O2﹣
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com