
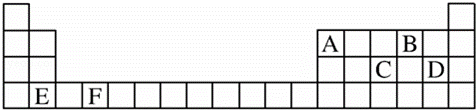
(1)A、B、C、D、E、F是元素周期表前四周期的元素,它们在元素周期表中的位置如图所示:
①写出F的基态原子的核外电子排布式:
②C元素的第一电离能比同周期相邻的两种元素的第一电离能都高的原因是 .
(2)A、B、C 3种元素中,A的第一电离能最小,C的电负性最大,3种元素的失电子能力由强到弱的顺序为
.
(3)D、E两种元素形成的化合物化学式为 .
考点: 元素周期律和元素周期表的综合应用.
分析: 由元素在周期表中位置,可知A为硼、B为氧、C为磷、D为Cl、E为Ca、F为Ti,
(1)①F为Ti,原子核外电子数为22,根据能量最低原理书写核外电子排布;
②P原子3p能级容纳3个电子,为半满稳定状态,能量较低;
(2)第一电离能越小,越容易失去电子,电负性越大越容易获得电子;
(3)D、E两种元素形成的化合物为氯化钙.
解答: 解:由元素在周期表中位置,可知A为硼、B为氧、C为磷、D为Cl、E为Ca、F为Ti,
(1)①F为Ti,原子核外电子数为22,由能量最低原理,其核外电子排布为:1s22s22p63s23p63d24s2,
故答案为:1s22s22p63s23p63d24s2;
②磷原子的最外层电子排布式3s23p3,3p能级容纳3个电子,它处于半充满稳定状态,能量较低,第一电离能高于同周期相邻元素,
故答案为:磷原子的最外层电子排布式3s23p3,3p能级容纳3个电子,它处于半充满稳定状态,能量较低;
(2)B、P、O 3种元素中,B的第一电离能最小,O的电负性最大,第一电离能越小,越容易失去电子,电负性越大越容易获得电子,故失去电子能力:B>P>O,
故答案为:B>P>O;
(3)D、E两种元素形成的化合物为氯化钙,其化学式为CaCl2,
故答案为:CaCl2.
点评: 本题是对物质结构的考查,题目难度中等,涉及核外电子排布、电离能、电负性等知识,注意理解同周期元素中第一电离能突跃原因,理解电离能与元素化合价关系.


科目:高中化学 来源: 题型:
下列化学方程式中有一个与其他三个在分类上不同,这个反应是()
A. 3Fe+2O2 Fe3O4
Fe3O4
B. C+CO2 2CO
2CO
C. NH4HCO3 NH3↑+H2O+CO2↑
NH3↑+H2O+CO2↑
D. Na2CO3+CO2+H2O═2NaHCO3
查看答案和解析>>
科目:高中化学 来源: 题型:
有机物甲、乙、丙、丁都是由C、H、O三种元素组成且也都只含有一种官能团.实验证明,丁氧化可得丙,乙氧化可以得到丙或丁,甲水解得乙和丙.假如用M表示物质的摩尔质量,则下列各式中正确的是( )
|
| A. | M(丙)>M(丁)>M(乙) | B. | M(丙)>M(乙)>M(丁) | C. | M(甲)=M(乙)+M(丙) | D. | 2M(丁)=M(乙)+M(丙) |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是()
A. SiH4比CH4稳定
B. O2﹣半径比F﹣的小
C. Na和Cs属于第 IA族元素,Cs失电子能力比Na强
D. P和As属于第 VA族元素,H3PO4酸性比H3AsO4弱
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期金属元素甲~戊在元素周期表中的相对位置如图所示.下列判断正确的是()
甲 乙
丙 丁 戊
A. 原子半径:丙<丁<戊 B. 金属性:甲>丙
C. 氢氧化物碱性:丙>丁>戊 D. 最外层电子数:甲>乙
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验操作均要用玻璃棒,其中玻璃棒用作引流的是()
①过滤 ②蒸发 ③溶解 ④向容量瓶转移液体.
A. ①和② B. ①和③ C. ③和④ D. ①和④
查看答案和解析>>
科目:高中化学 来源: 题型:
根据氧化物能否与酸或碱反应生成盐和水的性质,可把氧化物分为碱性氧化物、酸性氧化物、两性氧化物和不成盐氧化物,这种分类方法称为 分类法(填“交叉”或“树状”).
查看答案和解析>>
科目:高中化学 来源: 题型:
用物质的量都是0.1mol的CH3COOH和CH3COONa配制成1L混合溶液,已知其中c(CH3COO﹣)>c(Na+),对该混合溶液的下列判断正确的是()
A. cCH3COOH)+c(CH3COO﹣)=0.2 mol/L
B. c(OH﹣)>C(H+)
C. c(CH3COOH)>c(CH3COO﹣)
D. c(CH3COO﹣)+c(OH﹣)=0.2 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com