
分析 (1)CO2与H2反应生成CH3OH和H2O,根据原子守恒配平书写方程式;
(2)由题意可知,发生反应:2CO+SO2=S+2CO2,根据盖斯定律,①-②-③可得CO与SO2反应的热化学方程式;
(3)发生反应:CH4(g)+2NO2(g)=CO2(g)+N2(g)+2H2O(g),根据盖斯定律可知,①-②可得热化学方程式.
解答 解:(1)CO2与H2反应生成CH3OH和H2O,根据原子守恒配后反应方程式为:CO2+3H2$\frac{\underline{\;一定条件\;}}{\;}$CH3OH+H2O,
故答案为:CO2+3H2$\frac{\underline{\;一定条件\;}}{\;}$CH3OH+H2O;
(2)由题意可知,发生反应:2CO+SO2=S+2CO2,
已知:①C(s)+O2(g)=CO2(g)△H1=-393.5kJ•mol-1
②CO2(g)+C(s)=2CO(g)△H2=+172.5kJ•mol-1
③S(s)+O2(g)=SO2(g)△H3=-296.0kJ•mol-1
根据盖斯定律,①-②-③可得CO与SO2反应的热化学方程式:2CO(g)+SO2(g)=S(s)+2CO2(g)△H=-270kJ•mol-1,
故答案为:2CO(g)+SO2(g)=S(s)+2CO2(g)△H=-270kJ•mol-1;
(3)发生反应:CH4(g)+2NO2(g)=CO2(g)+N2(g)+2H2O(g),根据盖斯定律可知,①-②可得热化学方程式:CH4(g)+2NO2(g)=CO2(g)+N2(g)+2H2O(g)△H=-957.3kJ•mol-1,
故答案为:CH4(g)+2NO2(g)=CO2(g)+N2(g)+2H2O(g)△H=-957.3kJ•mol-1.
点评 本题综合考查根据盖斯定律书写热化学方程式,为高频考点,侧重于学生的分析、计算能力的考查,难度不大,注意对盖斯定律的理解与应用.


 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案 海淀课时新作业金榜卷系列答案
海淀课时新作业金榜卷系列答案科目:高中化学 来源: 题型:选择题
| A. | KClO3=K++Cl-+3O2- | B. | K2CO3=2K++CO32- | ||
| C. | NaOH=Na++OH- | D. | NH4Cl=NH4++Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 上述参加反应的NH3和生成H2的体积之比为3:2 | |
| B. | 同温同压下,NH3、H2的密度之比为2:17 | |
| C. | 相同质量的NH3、H2分子数之比为17:2 | |
| D. | 同温同体积下,相同质量NH3、H2的压强之比为2:17 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  分散系的分类 | |
| B. | 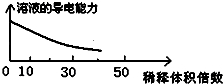 醋酸稀释 | |
| C. | 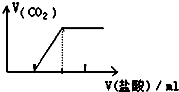 向Na2CO3溶液中逐滴滴入盐酸 | |
| D. | 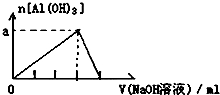 向AlCl3溶液中滴加过量的NaOH溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | M2+ | B. | M | C. | M3+ | D. | MO2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
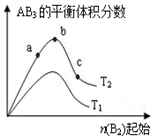 某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据如图判断:
某化学科研小组研究在其他条件不变时,改变某一条件对A2(g)+3B2(g)?2AB3(g)化学平衡状态的影响,得到如图所示的变化规律(图中T表示温度,n表示物质的量),根据如图判断:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com