
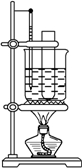
 实验室常用浓硝酸和浓硫酸的混合液与苯反应制取硝基苯.阅读下列材料回答有关问题.
实验室常用浓硝酸和浓硫酸的混合液与苯反应制取硝基苯.阅读下列材料回答有关问题.
| ||
| ||
 ;
; ;
;

科目:高中化学 来源: 题型:
| A、少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗 |
| B、眼睛里溅进了少量酸或碱溶液,要立即用大量水冲洗,边洗边眨眼睛 |
| C、不慎洒出的酒精在桌上燃烧起来,应立即用大量水扑灭 |
| D、将含硫酸的废液倒入水槽,用水冲入下水道 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 一定条件下,甲醇与水蒸气反应的化学方程式为:
一定条件下,甲醇与水蒸气反应的化学方程式为:| 4 |
| 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
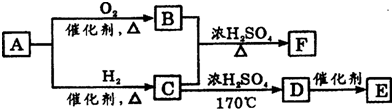
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 在一烧杯中盛有20g CaCl2和NaCl的混合固体粉末,向其中逐滴滴加溶质的质量分数为10.6%的Na2CO3溶液,生成沉淀的质量与所滴入Na2CO3溶液的质量关系曲线如图所示.请根据题意回答下列问题:
在一烧杯中盛有20g CaCl2和NaCl的混合固体粉末,向其中逐滴滴加溶质的质量分数为10.6%的Na2CO3溶液,生成沉淀的质量与所滴入Na2CO3溶液的质量关系曲线如图所示.请根据题意回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com