
2014年诺贝尔化学奖授予超高分辨率荧光显微镜的贡献者。人类借助于这种显微镜可以观察到单个的蛋白质分子。下列有关叙述不正确是

A.蛋白质中含有碳、氢、氧、氮等元素
B.蛋白质属于高分子化合物
C.蛋白质可完全水解生成氨基酸
D.消毒过程中细菌蛋白质发生了盐析
科目:高中化学 来源:2014-2015学年山东省潍坊市高三12月月考化学试卷(解析版) 题型:填空题
(12分)硼镁泥是一种工业废料,主要成份是MgO(占40%),还有CaO、MnO、Fe2O3、FeO、Al2O3、SiO2等杂质,以此为原料制取的硫酸镁,可用于印染、造纸、医药等工业。从硼镁泥中提取MgSO4·7H2O的流程如下:

根据题意回答下列问题:
(1)实验中需用1 mol·L-1的硫酸80mL,若用98%的浓硫酸来配制,除量筒、玻璃棒外,还需要的玻璃仪器有 。
(2)加入的NaClO可与Mn2+反应产生MnO2沉淀,该反应的离子方程式: 。
(3)在调节pH=5~6之前,还有一种离子也会被NaClO氧化,该反应的离子方程式为: 。
(4)如何检验滤液中Fe3+是否被除尽,简述检验方法 。
(5)已知MgSO4、CaSO4的溶解度如下表:
温度(℃) | 40 | 50 | 60 | 70 |
MgSO4 | 30.9 | 33.4 | 35.6 | 36.9 |
CaSO4 | 0.210 | 0.207 | 0.201 | 0.193 |
“除钙”是将MgSO4和CaSO4混合溶液中的CaSO4除去,根据上表数据,简要说明主要操作步骤 、 。
(6)如果提供的硼镁泥共100 g,得到的MgSO4·7H2O 196.8 g,则MgSO4·7H2O的产率为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江西省新余市高三上学期期末考试理综化学试卷(解析版) 题型:实验题
(14分)碱式碳酸镁有多种不同的组成,如:Mg2(OH)2CO3、Mg4(OH)2(CO3)3、Mg5(OH)2(CO3)4等。某研究性学习小组的同学们为了确定某碱式碳酸镁的组成,设下图所示的实验装置。

(1)实验步骤:
①按上图(夹持仪器未画出)组装好置后,首先进行的操作是________。E处干燥管盛放的药品是________________。
②称取碱式碳酸镁样品m1g,并将其放入硬质玻璃管中;
称量:装浓硫酸的洗气瓶C的质量为m2g;装碱石灰的U形管D的质量为m3g
③打开活塞___________,关闭__________缓缓鼓入空气数分钟。
④关闭活塞_______,打开__________,点燃酒精灯加热,待不再产生气体为止。
⑤打开活塞K1,缓缓鼓入空气数分钟,然后拆下装置,称得洗气瓶C的质量为m4g;U形管D的质量为m5g。实验测得数据如下:m1 = 31g ,m2 =87.6g ,m3 = 74.7g,m4 = 89.4g ,m5 = 87.9g,计算推导:该碱式碳酸镁的化学式为_________________。
(2)关于该实验方案,以下说法你认为正确的是______________(填字母)
A.硬质玻璃管中有水凝结对测定结果有较大影响
B.不称量碱式碳酸镁样品的质量无法确定碱式碳酸镁的组成
C.该实验装置也可用于确定天然碱[aNa2CO3·bNaHCO3·cH2O(a、b、c为正整数)]的化学组成
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南通市高三第一次模拟化学试卷(解析版) 题型:选择题
探究氨气及铵盐性质的过程中,下列根据实验现象得出的结论不正确的是

A.将集有氨气的试管倒扣于水槽中,液体迅速充满试管,说明氨气极易溶于水
B.将pH=11的氨水稀释1000倍,测得pH > 8,说明NH3·H2O为弱碱
C.加热NH4HCO3固体,观察到固体逐渐减少,试管口有液滴产生,说明NH4HCO3受热不稳定
D.将红热的Pt丝伸入上图所示的锥形瓶中,瓶口出现少量红棕色气体,说明氨气的氧化产物为NO2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南通市高三第一次模拟化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值。下列说法正确的是
A.0.1 mol溴苯中含有双键的数目为0.3NA
B.0.1 mol/L醋酸溶液中含有醋酸分子的数目为0.1 NA
C.5.6g Fe与足量的水蒸气完全反应,转移电子的数目为0.2NA
D.标准状况下,11.2L 由H2和CO组成的混合气体中含有分子的数目为0.5NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省枣阳市高三上学期期末考试理综化学试卷(解析版) 题型:填空题
(14分)硫酸镁在医疗上具有镇静、抗挛等功效。以菱镁矿(主要成分是MgCO3)为主要原料制备硫酸镁的方法如下:
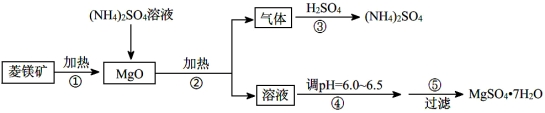
请回答下列问题:
(1)步骤②中发生反应的离子方程式为 。
(2)步骤④中调节pH=6.0~6.5的目的是 。
(3)对MgSO4·7H2O晶体直接加热 (填“能”或“不能”)得到无水MgSO4固体。
(4)步骤⑤的操作为 。
(5)长时间加热MgCO3悬浊液后生成Mg(OH)2,该反应的化学方程式为
(6)已知酸碱指示剂百里酚蓝变色的pH范围如表所示:
pH | < 8.0 | 8.0 ~ 9.6 | > 9.6 |
颜色 | 黄色 | 绿色 | 蓝色 |
25℃时,向Mg(OH)2的饱和溶液中滴加2滴百里酚蓝指示剂,溶液所呈现的颜色为 [25℃时,Mg(OH)2的溶度积Ksp=5.6×10-12]。
(7)药品A是中和胃酸的常用药物,其有效成分是铝和镁的碱式碳酸盐。现进行如下实验确定其化学式:
实验一:取该碱式碳酸盐3.01g充分灼烧至恒重,测得固体质量减少了1.30g;
实验二:另取该碱式碳酸盐3.01g使其溶于足量的盐酸中,产生CO2的体积为112mL(标准状况);
实验三:向实验二的溶液中加入足量的NaOH溶液得到1.74g白色沉淀。
该药品的化学式为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省枣阳市高三上学期期末考试理综化学试卷(解析版) 题型:选择题
分子式为C3H2Cl6的同分异构体共有(不考虑立体异构)
A.3种 B.4种 C.5种 D.6种
查看答案和解析>>
科目:高中化学 来源:2014-2015学年福建省漳州市八校高三第二次联考化学试卷(解析版) 题型:填空题
(14分)下图是实验室制备氯气并进行一系列相关实验的装置(夹持及加热仪器已略)。
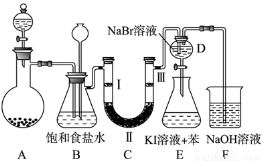
(1)制备氯气选用的药品为固体二氧化锰和浓盐酸,则相关的化学反应方程式为: 。装置B中饱和食盐水的作用是 ;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象 。
(2)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入 。
a | b | c | d | |
Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
Ⅱ | 碱石灰 | 硅胶 | 浓硫酸 | 无水氯化钙 |
Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(3)设计装置D、E的目的是比较氯、溴、碘单质的氧化性强弱。当向D中缓缓通入少量氯气时,可以看到无色溶液逐渐变为 色,打开活塞,将装置D中少量溶液加入装置E中,振荡。观察到的现象是 。
(4)装置F中用足量的NaOH溶液吸收余氯,试写出相应的离子方程式: 。
(5)如果将过量二氧化锰与20 mL 12 mol·L-1的浓盐酸混合加热,充分反应后生成的氯气 0.06 mol。(填“大于”“小于”“等于”),若有17.4 g的MnO2被还原,则被氧化的HCl的质量为 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年安徽省淮北市高三第一次模拟考试化学试卷(解析版) 题型:填空题
(14分)硼及其化合物在工业生产中应用广泛。用硼镁矿(主要成分Mg2B2O5.H2O)采用碳铵法生产硼酸主要流程如下:


(1)硼镁矿焙烧时需要粉碎,其目的是 。硼镁矿焙烧过程中只生成两种物质,写出化学方程式 。
(2)硼酸溶解度如下所示,从NH4H2BO3溶液获得硼酸晶体蒸发浓缩、冷去结晶、过滤、洗涤、干燥获得硼酸晶体。洗涤过程中需要用 (填“冷水”或“热水”),你的理由是 。
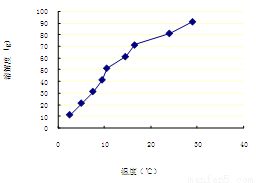
(3)测得硼酸晶体纯度的试验方法是,取0.5000g样品与锥形瓶中,加甘油和刚冷却的废水,微热使样品溶解,迅速冷却至室温,加酚酞指示剂,用NaOH标准溶液滴定至15.80ml时,溶液恰好显粉红色且半分钟不褪色。
已知:每1.00mlNaOH滴定液相当于30.92mg的H3BO3
①迅速冷却锥形瓶中溶液的方法是 ;
②滴定实验中加入甘油的目的 ;
③测该样品中H3BO3的质量分数为 ;
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com