
工业废水中常含有一定量Cr2O72-和CrO42-,它们会对人类及生态系统产生很大伤害。
已知:i. 2CrO42-(黄色)+ 2H+  Cr2O72-(橙色)+ H2O
Cr2O72-(橙色)+ H2O
ii. Cr(OH)3(s) + H2O  [Cr(OH)4]- (亮绿色) + H+
[Cr(OH)4]- (亮绿色) + H+
(1) 含铬工业废水的一种处理流程如下:

① i. 若在转化一步中调节溶液的pH=2,则溶液显_______色。
ii. 能说明转化一步反应达平衡状态的是_______(填字母序号)。
a.Cr2O72-和CrO42-的浓度相同 b.ν正(Cr2O72-) = 2ν逆(CrO42-)
c.溶液的颜色不变 d.溶液的pH不变
② 步骤②还原一步的离子方程式是___________________________;若还原l mol Cr2O72-离子,需要FeSO4·7H2O的物质的量是_______mol。
③ 沉淀一步中,向含Cr3+(紫色)溶液中,逐渐滴加NaOH溶液。当pH=4.6时,开始出现灰绿色沉淀,随着pH的升高,沉淀量增多。当pH≥13时,沉淀逐渐消失,溶液变为亮绿色。
i. 请解释溶液逐渐变为亮绿色的原因:_______。
ii. 若向0.05mol·L-1的Cr2(SO4)3溶液50mL中,一次性加入等体积0.6 mol·L-1的NaOH溶液,充分反应后,溶液中可观察到的现象是__________。
④ 在K[Cr(OH)4]和K2Cr2O7混合溶液中加入足量H2SO4酸化,铬元素以_______形式存在(填离子符号)。
(2) 用Fe做电极电解含Cr2O72-的酸性工业废水,可以直接除去铬。随着电解进行,在阴极附近溶液pH升高,产生Cr(OH)3沉淀。
① 结合上述工业流程分析用Fe做电极的原因:_______。
② 结合电极反应式解释在阴极附近溶液pH升高的原因:_______。
③ 溶液中同时生成的沉淀可能还有_______(填化学式)。
科目:高中化学 来源:2017届河北省高三下学期第二次质检考试理科综合化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的数值。下列有关叙述正确的是( )
A. 标准状况下,22.4LCCl4中所含C—C1键的数目为4NA
B. 在含Al3+总数为NA的AlCl3溶液中,Cl-总数为3NA
C. 向密闭容器中充入1molN2O4,加热使之充分分解,生成NO2的分子数为2NA
D. 7.8gNa2O2中阴离子所含的电子数为1.8NA
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省枣庄市北校区高一下学期第一次月考化学试卷(解析版) 题型:选择题
下列说法正确的是
A. 第2周期元素从左到右,最高正化合价从+1递增到+7
B. 在周期表中的过渡元素中寻找半导体材料
C. 元素周期表中元素的性质与元素在周期表中的位置有关
D. 同种元素的原子均有相同的质子数和中子数
查看答案和解析>>
科目:高中化学 来源:2017届安徽省安庆市高三第二次模拟考试理科综合化学试卷(解析版) 题型:简答题
SO2虽是大气污染物之一,但也是重要的工业原料,某同学在实验室设计如下实验,对SO2的部分性质进行了探究。
(1)二氧化硫的水溶液
①SO2易溶于水,常温常压下溶解度为1:40,其中有H2SO3生成。向SO2的饱和溶液中加入NaHSO3固体,有气体冒出,原因是__________。(结合有关平衡方程式简要说明)
②欲验证酸性:H2SO3>HClO,选用下面的装置,其连接顺序为:
A ________(按气流方向用大写字母表示即可)。能证明H2SO3的酸性强于HClO的实验现象为___。
________(按气流方向用大写字母表示即可)。能证明H2SO3的酸性强于HClO的实验现象为___。
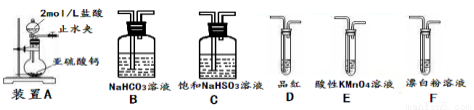
(2)二氧化硫的还原性
已知SO2具有还原性,可以还原I2,可以与Na2O2发生反应,按图示装置进行实验。(部分固定装置未画出)

操作步骤 | 实验现象 | 解释原因 |
关闭弹簧夹2,打开弹簧夹1,注入硫酸至浸没三颈烧瓶中固体 | 若将带火星的木条放在D试管口处,木条不复燃 | SO2与Na2O2反应无O2生成,可能发生的化学反应方程式为①____ |
若将带火星的木条放在D试管口处,木条复燃 | SO2与Na2O2反应有O2生成,发生的化学反应为:2SO2+2Na2O2=2Na2SO3+O2 | |
关闭弹簧夹1,打开弹簧夹2,残余气体进入E,F中。 | E中②__________ | E中反应的离子方程式③________ |
F中④__________ | F中反应为2OH-+SO2=SO32-+H2O |
查看答案和解析>>
科目:高中化学 来源:2017届安徽省安庆市高三第二次模拟考试理科综合化学试卷(解析版) 题型:选择题
化学与生产、生活、社会密切相关,下列有关说法中正确的是
A. 煤炭经气化、液化和干馏等处理后,可转化为清洁能源
B. “绿蚁新醅酒,红泥小火炉”,“新醅酒”即新酿的酒,在酿酒的过程中,葡萄发生了水解反应
C. 地沟油和矿物油的主要化学成分相同
D. 聚氯乙烯可以用作食品包装袋
查看答案和解析>>
科目:高中化学 来源:2017届内蒙古赤峰市宁城县高三一模理科综合化学试卷(解析版) 题型:选择题
设NA为阿伏加德罗常数的值,下列说法正确的是
A. 标准状况下,22.4 L空气中O2、N2分子总数目为NA
B. 0.1 mol羟基中所含电子数目为NA
C. 28 g乙烯、丙烯混合气体中所含原子数为6NA
D. 5.6 g铁与硝酸完全反应时转移的电子数目为0.3NA
查看答案和解析>>
科目:高中化学 来源:2016届湖南省高三2月模拟理科综合化学试卷(解析版) 题型:选择题
人体吸入CO后在肺中发生反应 导致人体缺氧。向某血样中通 入CO与O2的混合气
导致人体缺氧。向某血样中通 入CO与O2的混合气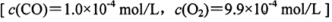 ,氧合血红蛋白 HbO2浓度随时间变化曲线如下图所示。下列说法正确的是
,氧合血红蛋白 HbO2浓度随时间变化曲线如下图所示。下列说法正确的是
A. 反应开始至4s内用HbO2表示的平均反应速率为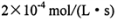
B. 反应达平衡之前,O2与HbCO的反应速率逐渐减小
C. 将CO中毒病人放入高压氧舱治疗是利用了化学平衡移动原理
D. 该温度下反应 的平衡常数为107
的平衡常数为107
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省高二2月联考化学试卷(解析版) 题型:选择题
用石墨作电极完全电解含1 mol溶质X的溶液后,向溶液中加入一定量的物质Y能使电解液恢复到起始状态是
选项 | X溶液 | 物质Y |
A | CuCl2 | 1 mol Cu(OH)2 |
B | KOH | 1 mol KOH |
C | Na2SO4 | 1 mol H2SO4 |
D | AgNO3 | 0.5 mol Ag2O |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源:2017届四川省成都市高三第二次模拟考试理综化学试卷(解析版) 题型:选择题
下列选项中,利用相关实验器材(规格和数量不限)能够完成相应实验的是
选项 | 实验器材 | 相应实验 |
A | 试管、铁架台、导管 | 乙酸乙酯的制备 |
B | 锥形瓶、漏斗、双孔塞、导管、带余烬的木条、药匙 | 检验MnO2对H2O2分解速率的影响 |
C | 500mL容量瓶、烧杯、玻璃棒、天平 | 配制 500mL1.00mol/LNaCl溶液 |
D | 三脚架、坩埚、酒精灯、坩埚钳 | 钠在空气中燃烧 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com