
 中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%.
中国政府承诺,到2020年,单位GDP二氧化碳排放比2005年下降40%~50%.| 温度/℃ | 0 | 100 | 200 | 300 | 400 |
| 平衡常数 | 667 | 13 | 1.9×10-2 | 2.4×10-4 | 1×10-5 |
分析 (1)要求制氢方法最节能,可从节能的角度分析;
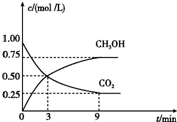
(2)①根据v=$\frac{△c}{△t}$计算从3min到9minv(H2);
②化学反应达到平衡状态时正逆反应速率相等,各物质的浓度不变,由此衍生的物理量不变;
(3)A.依据平衡常数随温度变化和平衡移动原理分析判断;
B.升高温度后正逆反应速率都增大;
C.结合平衡三段式列式计算,平衡常数等于生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积;
D.正反应吸热,温度越低反应物转化率越高.
解答 解:(1)电解水、高温以及天然气的使用都会消耗能源,不符合低碳要求,使用太阳能可减小低碳,故C正确,
故答案为:C;
(2)①从4min到10min,v(CO2)=$\frac{0.50mol/L-0.25mol/L}{10min-4min}$,则v(H2)=3v(CO2)=3×$\frac{0.50mol/L-0.25mol/L}{10min-4min}$=0.125mol/(L•min)-1,
故答案为:0.125;
②A.反应中CO2与CH3OH的物质的量浓度之比为1:1时,没有达到平衡状态,故A错误;
B.由于气体的总质量不变,容器的体积不变,则无论是否达到平衡状态,气体的密度都不变,故B错误;
C.化学反应速率之比等于化学计量数之比,无论是否达到平衡状态,都存在单位时间内每消耗3molH2,同时生成1molH2O,故C错误;
D.CO2的体积分数在混合气体中保持不变,说明达到平衡状态,故D正确;
故答案为:D;
(3)A.依据平衡常数随温度变化和平衡移动原理分析判断,随温度升高平衡常数减小,正反应为放热反应,故A正确;
B.该反应为放热反应,升高温度时平衡向着逆向移动,CH3OH(g)的体积分数减小,但v正(CH3OH)和v逆(CH3OH)都增大,故B错误;
C.结合平衡三段式列式计算,平衡常数等于生成物平衡浓度幂次方乘积除以反应物平衡浓度幂次方乘积,
CO(g)+2H2(g)?CH3OH(g)
起始量(mol/L) 0.1 0.2 0
变化量(mol/L) 0.1×50% 0.1 0.05
平衡量(mol/L) 0.05 0.1 0.05
该稳定性该飞跃的平衡常数为:K=$\frac{0.05}{0.05×0.{1}^{2}}$=100,故C正确;
D、工业上采用稍高的压强(5MPa)和250℃,是从转化率和反应速率两方面综合考虑,故D错误;
故答案为:AC.
点评 本题考查化学平衡的计算,题目难度中等,涉及化学平衡常数、化学反应速率的计算、化学平衡状态的判断、环境污染及治理等知识,明确化学平衡及其影响为解答关键,注意掌握三段式在化学平衡计算中的应用,试题培养了学生的分析能力及化学计算能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | 在一定条件下,苯与液溴、硝酸作用生成溴苯、硝基苯的反应都属于取代反应 | |
| B. | 戊烷有4种同分异构体,它们熔点、沸点各不相同 | |
| C. | 油脂发生皂化反应可以得到高级脂肪酸盐与甘油 | |
| D. | 淀粉和蛋白质都属于高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2+2NaOH═Na2SiO3+H2O | B. | H2SiO3$\frac{\underline{\;\;△\;\;}}{\;}$SiO2+H2O | ||
| C. | Na2SiO3+CO2+H2O═H2SiO3+Na2CO3 | D. | SiO2+CaCO3$\frac{\underline{\;高温\;}}{\;}$CaSiO3+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO燃烧的热化学方程式为2CO(g)+O2(g)═2CO2(g)△H=-282.8kJ•mol-1 | |
| B. | H2燃烧的热化学方程式为2H2(g)+O2(g)═2H2O(g)△H=-571.6kJ•mol-1 | |
| C. | 燃烧前混合气体中CO的体积分数为40% | |
| D. | 燃烧后的产物全部与足量的过氧化钠作用可产生0.125mol O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2H2(g)+O2(g)═2H2O(l)△H1 2H2(g)+O2(g)═2H2O(g)△H2 | |
| B. | S(g)+O2(g)═SO2 (g)△H1 S(s)+O2(g)═SO2 (g)△H2 | |
| C. | C(s)+O2(g)═CO(g)△H1 C(s)+O2(g)═CO2(g)△H2 | |
| D. | HCl(g)═H2(g)+Cl2(g)△H1 2HCl(g)═H2(g)+Cl2(g)△H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫酸、干冰、纯碱 | B. | 硝酸、二氧化硫、苛性钠 | ||
| C. | 盐酸、氧化铜、熟石灰 | D. | 醋酸、水、烧碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 胶体区别于其他分散系的本质特征是分散质的微粒直径在10-5:10-7m之间 | |
| B. | 光线透过胶体时,胶体中可发生丁达尔效应 | |
| C. | Fe(OH)3胶体能够使水中悬浮的固体颗粒沉降,达到净水目的 | |
| D. | 用平行光照射NaCl溶液和Fe(OH)3胶体时,产生的现象相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com