
分析 (1)最长的主链含有8个C原子,甲基处于2、6号碳原子上,乙基处于4号碳原子上,据此书写,在核磁共振氢谱中的吸收峰数,根据氢原子种类判断;
(2)二烯烃的命名中选取含有2个碳碳双键的碳链为主链,距离碳碳双键最近的一端命名为1号碳,该有机物结构对称,核磁共振氢谱有2组峰,据此解答即可.
解答 解:(1)2,6-二甲基-4-乙基辛烷中最长的主链含有8个C原子,甲基处于2、6号碳原子上,乙基处于4号碳原子上,其结构简式为CH3CH(CH3)CH2CH(CH2CH3)CH2CH(CH3)CH2CH3,连在同一碳上的甲基上的氢为等效氢,该有机物含11种H,核磁共振氢谱有11组峰,
故答案为:CH3CH(CH3)CH2CH(CH2CH3)CH2CH(CH3)CH2CH3;11;
(2)2,5-二甲基-2,4-己二烯,主链为2,4-己二烯,在2号C、5号C上都含有一个甲基,编号从距离碳碳双键最近的一端开始,该有机物结构简式为C(CH3)2=CHCH=C(CH3)2,该有机物结构对称,含2种H,核磁共振氢谱有2组峰,
故答案为:C(CH3)2=CHCH=C(CH3)2;2.
点评 本题考查有机物的命名、有机物结构简式的书写、有机物结构中氢原子种类,题目难度不大,注意掌握有机物的命名原则.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 离子半径:W>Z>X | B. | 单质熔点:W>Z | ||
| C. | 最高正价:W>X>Y>Z | D. | 原子序数:Z>W>X>Y |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| 物质 | 价格/元?吨-1 |
| 漂液(含25.2%NaClO) | 450 |
| 双氧水(含30%H2O2) | 2400 |
| 烧碱(含98%NaOH) | 2100 |
| 纯碱(含99.5%Na2CO3) | 600 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
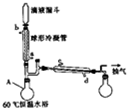 过氧乙酸常用作氧化剂和灭菌剂,实验室合成过氧乙酸并测定其含量的相关步骤如下:
过氧乙酸常用作氧化剂和灭菌剂,实验室合成过氧乙酸并测定其含量的相关步骤如下: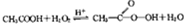
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol任何物质都含有约6.02×1023个原子 | |
| B. | 气体摩尔体积在非标准状况下也有可能是22.4L/mol | |
| C. | 在使用摩尔表示物质的量的单位时,应用化学式指明粒子的种类 | |
| D. | 物质的量是国际单位制中七个基本物理量之一 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com