
| A、气体摩尔体积L/g |
| B、摩尔质量g/mol |
| C、物质的量浓度mol/L |
| D、物质的量 mol |


科目:高中化学 来源: 题型:
| A、乙烯与溴的四氯化碳反应制1,2-二溴乙烷 |
| B、苯与溴水混合、充分振荡后,静置,溴水层褪色 |
| C、苯与浓硝酸、浓硫酸混合共热制取硝基苯 |
| D、在一定条件下苯与氢气反应制取环己烷 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分散质粒子的直径在10-9~10-7m之间的分散系叫做胶体 |
| B、KAl(SO4)2在水溶液中电离方程式为KAl(SO4)2═K++Al3++SO42- |
| C、利用丁达尔效应可以鉴别CuSO4溶液和氢氧化铁胶体 |
| D、氯气可用于自来水的消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、加催化剂,V正和V逆都发生变化,且变化的倍数相等 |
| B、增大压强,V正和V逆都增大,且V正增加倍数大于V逆增加倍数 |
| C、降低温度,V正和V逆都减少,且V逆减少倍数大于V正减少倍数 |
| D、通入氩气,V正和V逆都增大,且V正增加倍数大于V逆增加倍数 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分别充满HCl、NH3的烧瓶倒置于水中后液面迅速上升,说明二者均易溶于水 | ||||||
B、向NH4HCO3溶液中加过量的NaOH溶液并加热,离子方程式为:NH
| ||||||
| C、用NH4Cl固体和Ca(OH)2固体制备并收集NH3,需要的玻璃仪器有酒精灯、大试管、导管、集气瓶 | ||||||
| D、用湿润的红色石蕊试纸检验氨气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 A、B、C、D是中学化学的常见物质,其中A、B、C均含有同一种元素.在一定条件下相互转化的关系如下图所示(部分反应中的H2 O已略去).请填空:
A、B、C、D是中学化学的常见物质,其中A、B、C均含有同一种元素.在一定条件下相互转化的关系如下图所示(部分反应中的H2 O已略去).请填空:查看答案和解析>>
科目:高中化学 来源: 题型:
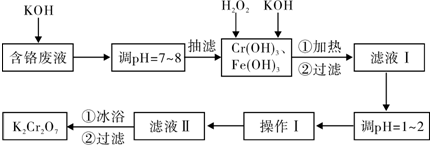
| 物质 | 0℃ | 20℃ | 40℃ | 60℃ | 80℃ | 100℃ |
| KCl | 28.0 | 34.2 | 40.1 | 45.8 | 51.3 | 56.3 |
| K2SO4 | 7.4 | 11.1 | 14.8 | 18.2 | 21.4 | 24.1 |
| K2Cr2O7 | 4.7 | 12.3 | 26.3 | 45.6 | 73.0 | 102.0 |
| KNO3 | 13.9 | 31.6 | 61.3 | 106 | 167 | 246.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com