
 ;
; .
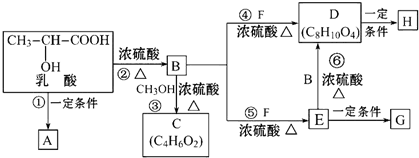
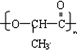
. 分析 A、H、G为链状高分子化合物,乳酸中含有羧基和醇羟基,能发生缩聚反应生成高分子化合物,且A是链状高分子化合物,则A结构简式为 ;
;
乳酸在浓硫酸作用下发生消去反应生成B,B为CH2═CHCOOH,CH2═CHCOOH与甲醇发生酯化反应生成C,则C为CH2═CHCOOCH3;F为HO-CH2CH2-OH,B和F发生酯化反应,1molF和与1molB或2molB发生酯化反应,由D的化学式可知,F和2molB完全发生酯化反应,则D为CH2═CHCOOCH2CH2OOCCH═CH2,1molB和1molF发生酯化反应,则E为CH2=CHCOOCH2CH2OH,D和E都含有C=C,在一定条件下都可发生加聚反应,H的结构简式为 ,G的结构简式为
,G的结构简式为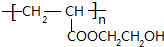 ,据此分析解答.
,据此分析解答.
解答 解:A、H、G为链状高分子化合物,乳酸中含有羧基和醇羟基,能发生缩聚反应生成高分子化合物,且A是链状高分子化合物,则A结构简式为 ;
;
乳酸在浓硫酸作用下发生消去反应生成B,B为CH2═CHCOOH,CH2═CHCOOH与甲醇发生酯化反应生成C,则C为CH2═CHCOOCH3;F为HO-CH2CH2-OH,B和F发生酯化反应,1molF和与1molB或2molB发生酯化反应,由D的化学式可知,F和2molB完全发生酯化反应,则D为CH2═CHCOOCH2CH2OOCCH═CH2,1molB和1molF发生酯化反应,则E为CH2=CHCOOCH2CH2OH,D和E都含有C=C,在一定条件下都可发生加聚反应,H的结构简式为 ,G的结构简式为
,G的结构简式为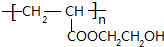 ,
,
(1)通过以上分析知,A的结构简式为 ,故答案为:
,故答案为: ;
;
(2)通过以上分析知,反应②的反应类型是消去反应,反应③的反应类型是酯化反应或取代反应,
故答案为:消去反应;酯化(取代)反应;
(3)E为CH2=CHCOOCH2CH2OH,其官能团名称是碳碳双键、酯基和羟基,
故答案为:碳碳双键、酯基、羟基;
(4)该反应方程式为酸和醇的酯化反应,反应方程式为CH2=CHCOOH+HOCH2CH2OH$→_{△}^{浓硫酸}$CH2=CHCOOCH2CH2OH+H2O,
故答案为:CH2=CHCOOH+HOCH2CH2OH$→_{△}^{浓硫酸}$CH2=CHCOOCH2CH2OH+H2O;
(5)E为CH2=CHCOOCH2CH2OH,一定条件下,E发生加聚反应生成G,反应方程式为 ,
,
故答案为: .
.
点评 本题考查有机物推断,为高频考点,侧重考查学生分析推断能力,以弱酸官能团及其性质为突破口结合反应条件、某些物质的分子式来进行推断,难点是有机化学知识的灵活运用,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 含有金属元素的离子一定是阳离子 | |
| B. | 金属阳离子被还原,一定得到金属单质 | |
| C. | 有单质参与的化合反应一定是氧化还原反应 | |
| D. | 在氧化还原反应中,非金属单质一定是氧化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
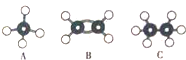 现有A、B、C三种烃,其球棍模型如图:
现有A、B、C三种烃,其球棍模型如图: .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向冰醋酸中加水至配成醋酸稀溶液的过程中H+的浓度逐渐减少 | |
| B. | 一定温度下,向一定量纯水中通入少量HCl气体后,水的电离平衡正向移动 | |
| C. | 中和等体积等物质的量浓度的氨水和NaOH溶液时,消耗等浓度的稀硫酸的体积氨水比NaOH溶液多 | |
| D. | 室温下,pH=5的硫酸铵和pH=9醋酸钠两溶液中,由水电离出的氢离子浓度相等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同系物的化学性质相似 | |
| B. | 同位素的化学性质几乎相同 | |
| C. | 相对分子质量相同的化合物,互称同分异构体 | |
| D. | 同素异形体之间的转化,同分异构体之间的转化都属于化学变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液中导电粒子的数目减少 | |
| B. | 溶液中$\frac{c(C{H}_{3}CO{O}^{-})•c({H}^{+})}{c(C{H}_{3}COOH)}$不变 | |
| C. | 醋酸的电离程度增大,c(H+)亦增大 | |
| D. | 再加入10mL pH=11的NaOH溶液,混合液pH=7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 蒸馏、分馏、干馏都属于物理变化 | |
| B. | 石油裂解可以得到氯乙烯 | |
| C. | 油脂水解可得到氨基酸和甘油 | |
| D. | 淀粉和纤维素的组成都是(C6H10O5)n,水解最终产物都是葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 热稳定性:HCl>H2S>PH3 | B. | 原子半径:Na<Mg<Cl | ||
| C. | 酸性强弱:H2SiO3<H2CO3<H2SO4 | D. | 碱性强弱:LiOH>NaOH>KOH |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com