
【题目】一定温度下,用Na2S沉淀Cu2+、Mn2+、Fe2+、Zn2+四种金属离子(M2+),形成沉淀所需S2-最低浓度的对数值lgc(S2-)与lgc(M2+)关系如图所示。下列说法不正确的是

A. 若向沉淀剂Na2S溶液通入HC1气体至中性,存在关系: c(HS-)+2c(H2S)=c(Cl-)
B. 该温度下,Ksp(MnS)大于1.0×10-35
C. 若将MnS、FeS的饱和溶液等体积混合,再加入足量的浓 Na2S溶液,发生的反应为MnS沉淀少于FeS
D. 向l00mL浓度均为10-5mol·L-1Zn2+、Fe2+、Mn2+的混合溶液中逐滴加入10-4mol·L-1Na2S溶液,ZnS先沉淀
【答案】D
【解析】
A、若向沉淀剂Na2S溶液通入HC1气体至中性,原溶液中存在物料守恒,c(Na+)=2c(S2-)+2c(HS-)+2c(H2S),通入HCl后溶液电荷守恒分析计算;
B、MnS饱和溶液中存在沉淀溶解平衡:MnS(s)![]() Mn2+(aq)+S2-(aq),据此书写计算即可
Mn2+(aq)+S2-(aq),据此书写计算即可
C、根据图象,FeS的图线在MnS的上方,则Ksp(FeS)>Ksp(MnS),溶液中亚铁离子浓度大。
D、同类型物质,溶度积小的优先产生沉淀;
A、若向沉淀剂Na2S溶液通入HC1气体至中性,若向沉淀剂Na2S溶液通入HC1气体至中性,原溶液中存在物料守恒,c(Na+)=2c(S2-)+2c(HS-)+2c(H2S),通入HCl后溶液电荷守恒c(H+)+c(Na+)=2c(S2-)+c(HS-)+c(OH-)+c(Cl-),带入计算得到c(Cl-)═c(HS-)+2c(H2S),故A正确;
B、MnS饱和溶液中存在沉淀溶解平衡:MnS(s)![]() Mn2+(aq)+S2-(aq),其溶度积常数为Ksp=c(Mn2+)c(S2-),根据图象,可计算FeS的Ksp数值为Ksp(FeS)=c(Fe2+)c(S2-)=1×10-20,CuS的Ksp数值为Ksp(CuS)=c(Cu2+)c(S2-)=1×10-35,MnS的图线在CuS的上方,因此MnS的溶度积常数大于CuS的溶度积常数,即Ksp(MnS)大于1.0×10-35,故B正确;
Mn2+(aq)+S2-(aq),其溶度积常数为Ksp=c(Mn2+)c(S2-),根据图象,可计算FeS的Ksp数值为Ksp(FeS)=c(Fe2+)c(S2-)=1×10-20,CuS的Ksp数值为Ksp(CuS)=c(Cu2+)c(S2-)=1×10-35,MnS的图线在CuS的上方,因此MnS的溶度积常数大于CuS的溶度积常数,即Ksp(MnS)大于1.0×10-35,故B正确;
C、根据图象,FeS的图线在MnS的上方,则Ksp(FeS)>Ksp(MnS), 若将MnS、FeS的饱和溶液等体积混合,Fe2+浓度大,再加入足量的浓 Na2S溶液,发生的反应为MnS沉淀少于FeS,故C正确;
D、 根据图象,ZnS的图线在MnS的上方,则Ksp(ZnS)>Ksp(MnS),向含Mn2+、Zn2+的稀溶液中滴加Na2S溶液,同类型物质,溶度积小的优先产生沉淀,因此先析出MnS沉淀,故D错误;
故选D。


科目:高中化学 来源: 题型:
【题目】如图是某研究性学习小组设计的对一种废旧合金各成分(含有Cu、Fe、Si三种成分)进行分离、回收再利用的工业流程,通过该流程能得到常用的单质、聚铁(碱式硫酸铁的聚合物)、铁红(Fe2O3)和绿矾(FeSO4·7H2O)。
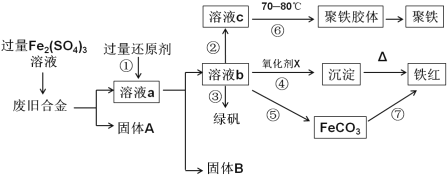
(1)①中过量的还原剂应是____________________。
(2) 向溶液b中加入酸性KMnO4溶液发生反应的离子方程式为_______________________。
(3)②中加入H2O2,并调节pH值得到溶液c,在⑥中,将溶液c控制到70-80℃的目的是________。
(4)在③中,蒸发浓缩需要的硅酸盐仪器除酒精灯外,还有_________________________。
(5)在④中的氧化剂X是________________________。
(6)在⑤中,向溶液b加入了NH4HCO3溶液,得到FeCO3沉淀,写出离子反应方程式 ______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学用以下装置制备并检验 Cl2的性质。下列说法正确的是( )

A.Ⅰ图:若 MnO2 过量,则浓盐酸可全部消耗完
B.Ⅱ图:证明新制氯水具有酸性和漂白性
C.Ⅲ图:产生了棕黄色的雾
D.Ⅳ图:日光照射烧瓶中的饱和氯水会有气泡产生,这是由于氯气光照条件下溶解度下降而逸出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组为探究浓硫酸和二氧化硫的性质,设计了如下图所示的装置进行实验(夹持装置已省略):

请回答:
(1)用“可抽动铜丝”代替“直接投入铜片”的优点是_____。
(2)说明SO2气体产生的实验现象是_____。装置⑤的作用是_____。
(3)为了验证SO2是酸性氧化物,③中可选择的试剂是_____。
A.澄清石灰水 B.饱和食盐水 C.碘水 D.品红溶液
(4)下列说法正确的是_____。
A.实验开始后,②和④中溶液均褪色,两者均可证明SO2具有漂白性
B.反应后,将①试管中的白色固体加入水中,溶液呈蓝色
C.先向装置中加入试剂(药品),再进行气密性检查
D.⑤中的NaOH溶液可用Na2CO3溶液代替
(5)若将抽动的铜丝换成炭块进行反应,写出反应的化学方程式_____;该反应体现浓硫酸的_____(选填“脱水性”“吸水性”“强氧化性”“酸性”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、I、W、Q在元素周期表中的相对位罝如下图所示,五种元素中有且只有一种金属元素。下列说法不正确的是

A. X与Y或W与Y所形成的化合物可能会引起相同的环境污染
B. 简单离子半径的大小:X>Y>Z>W>Q
C. Z的氢化物具有较强的还原性
D. 最高价含氧酸酸性:Q>W
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,A、B两个装置中的烧杯分别盛有足量的CuCl2溶液。

(1)A、B、C三个装置中属于原电池的是________(填标号,下同),属于电解池的是_____________
(2)A池中Zn是_____极,电极反应式为________;Cu是______极,电极反应式为______________,A中总反应的方程式为________________________。
(3)B池中总反应的方程式为________________。
(4)C池中Zn是____极,电极反应式为_____;Cu是______极,电极反应式为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质在水溶液中的电离方程式,正确的是( )
A.CH3COOH![]() H++CH3COO-B.KClO3=K++Cl-+3O2-
H++CH3COO-B.KClO3=K++Cl-+3O2-
C.H2CO3![]() 2H++CO32-D.NaHSO4=Na++HSO4-
2H++CO32-D.NaHSO4=Na++HSO4-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】恒温下,在容积固定的密闭容器中发生如下反应:aX(S)+bY(g) ![]() cZ(g)+dW(g) △H>0,下列叙述正确的是
cZ(g)+dW(g) △H>0,下列叙述正确的是
A. 平衡后继续充入X,正反应速率增大
B. 平衡后继续充入X,W的体积分数增大
C. 平衡后通入少量Y,平衡右移,△H增大
D. 恒温,恒容下充入1mol稀有气体He,Z的浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,将AgNO3溶液分别滴加到浓度均为0.01mol/L的NaBr、Na2SeO3溶液中,所得的沉淀溶解平衡曲线如图所示(Br-、SeO32-用Xn-表示,不考虑SeO32-的水解)。下列叙述正确的是

A. Ksp(Ag2SeO3)的数量级为10-10
B. d点对应的AgBr溶液为不饱和溶液
C. 所用AgNO3溶液的浓度为10-3 mol/L
D. Ag2SeO3(s)+2Br-(aq)==2AgBr(s)+SeO32- (aq)平衡常数为109.6,反应趋于完全
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com