
A��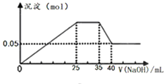 ��ʾ��Mg2+��Al3+��NH4+������Һ�еμ�NaOH��Һʱ������������NaOH������Ĺ�ϵͼ�����������ӵ����ʵ���֮��Ϊ��n��Mg2+����n��Al3+����n�� NH4+��=2��1��2������ʹ�õ�NaOH��Ũ��Ϊ2mol?L-1�� |
B��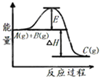 �����߱�ʾij��Ӧ���̵������仯��������A��g����B��g����Ӧ��������C��g��ʱ����H��0����ʹ����������Eֵ���С�� |
C��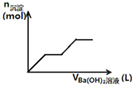 ��������ʾ�������ữ��MgSO4��Һ�м���Ba��OH��2��Һʱ���������������ʵ�����n�������Ba��OH��2��Һ�����V��֮��Ĺ�ϵͼ |
D��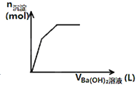 ��ʾ��һ��������������Һ�еμ�Ba��OH��2��Һʱ���������������ʵ�����n�������Ba��OH��2��Һ�����V��֮��Ĺ�ϵͼ |
| 0.025xmol-0.005��3xmol |
| 2 |


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ڢ� | B���ۢ� | C���ڢ� | D���٢� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
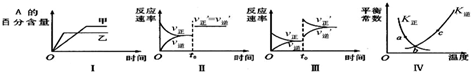
| A��ͼI��ʾ�¶ȶԻ�ѧƽ���Ӱ�죬�Ҽ��¶Ƚϸ� |
| B��ͼ���ʾt0ʱ����С��������Է�Ӧ���ʵ�Ӱ�� |
| C��ͼ���ʾt0ʱ������BŨ�ȶԷ�Ӧ���ʵ�Ӱ�� |
| D��ͼ����a��b��c������ֻ��b���Ѿ��ﵽ��ѧƽ��״̬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����淴Ӧ�Ļ�ѧ��������a��b+c |
| B��ѹ���������ݻ�ʱ��v������v����С |
| C���ﵽ��ƽ��ʱ��Y��ZŨ������Kֵ��� |
| D���ﵽ��ƽ���������������䣬��������Xƽ�������ƶ���X��ת�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
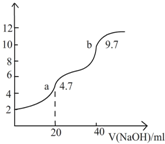 ��0.1000mol/LNaOH��Һ�ζ�20.00mlH2A��Һ��ʵ������ҺpH��NaOH��Һ����仯������ͼ��ʾ�������й�˵��������ǣ�������
��0.1000mol/LNaOH��Һ�ζ�20.00mlH2A��Һ��ʵ������ҺpH��NaOH��Һ����仯������ͼ��ʾ�������й�˵��������ǣ�������| A��H2A�����ʵ���Ũ��Ϊ0.1000mol��L-1 |
| B��H2A�Ƕ�Ԫ���� |
| C��a-b�η�����ӦHA-+OH-=H2O+A2- |
| D��a��ʱHA-��ˮ��̶ȴ��ڵ��̶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ֻ��Fe2+ |
| B��ֻ��Fe3+ |
| C��ֻ��Fe2+��Cu2+ |
| D��ֻ��Fe3+��Cu2+ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com