
| A. | 亚硫酸的酸性大于碳酸,故硫的非金属性大于碳 | |
| B. | 碳酸的酸性大于次氯酸,故碳的非金属性大于氯 | |
| C. | 硝酸的酸性大于硅酸,故氮的非金属性大于硅 | |
| D. | 氢氟酸的酸性大于氢氯酸,故氟的非金属性大于氯 |
分析 已知:元素的最高价氧化物的水化物酸性越强其非金属性就越强,则比较非金属性对应的酸应为最高价含氧酸,其它非最高价以及氢化物不能用于比较,以此解答该题.
解答 解:A.亚硫酸的酸性大于碳酸,但亚硫酸中S元素化合价为+4价,不是最高价,不能用于比较非金属性,故A错误;
B.次氯酸中Cl元素化合价为+1价,不是最高价,不能用于比较非金属性,故B错误;
C.硝酸、硅酸都是最高价氧化物的水化物,可用于比较,故C正确;
D.氢氟酸、氢氯酸都不是含氧酸,不能用于比较非金属性,故D错误.
故选C.
点评 本题考查元素周期表和周期律的综合应用,为高频考点,把握元素金属性与非金属性的比较方法为解答的关键,侧重规律性知识的考查,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 冒白雾,混合物温度升高 | B. | 产生黄绿色气体 | ||
| C. | 冒白雾,混合物温度降低 | D. | 液体四溅,冒白烟 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
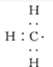 ;
;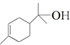 )的官能团的名称为碳碳双键、羟基;
)的官能团的名称为碳碳双键、羟基; 与溴发生加成反应的产物最多有4种,它们的结构简式为
与溴发生加成反应的产物最多有4种,它们的结构简式为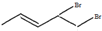 、
、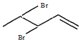 、
、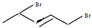 和
和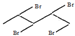 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 28gC2H4所含共用电子对数目为4NA | |
| B. | 1 mol碳正离子(CH3+)所含的电子总数为8 NA | |
| C. | 标准状况下,1L庚烷完全燃烧所生成的气态产物的分子数为(7/22.4)NA | |
| D. | 0.5mol 1,3-丁二烯分子中含有C=C双键数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2-氯丁烷在氢氧化钠的水溶液中加热有机产物仅有一种 | |
| B. | 2-丁醇消去反应的产物中有两种烯烃 | |
| C. | 检验氯乙烷中的氯元素,先加入氢氧化钠溶液加热,再加入几滴硝酸银溶液即可 | |
| D. | 2-甲基-2-丁醇可以发生消去反应,不能发生催化氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{z}^{y}$R | B. | ${\;}_{z}^{y+z}$R | C. | ${\;}_{z+x}^{y+z}$R | D. | ${\;}_{z+x}^{y+z+x}$R |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C3N4晶体是分子晶体 | |
| B. | C 原子sp3杂化,与4个处于4面体顶点的N 原子形成共价键 | |
| C. | C3N4晶体中C、N原子个数之比为4:3 | |
| D. | C3N4晶体中粒子间通过离子键结合 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com