
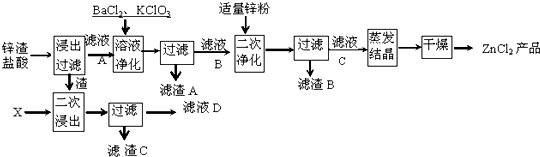


科目:高中化学 来源: 题型:
| A、H+、Ca2+、Fe3+、NO3- |
| B、Ba2+、Cl-、Al3+、H+ |
| C、Na+、NH4+、I-、HS- |
| D、Na+、NH3?H2O、K+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HF、HCl、HBr、HI的热稳定性依次减弱 |
| B、NaF、NaCl、NaBr、NaI的熔点依次降低 |
| C、F2、Cl2、Br2、I2的熔沸点逐渐升高 |
| D、H2S的熔沸点小于H2O的熔沸点 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、2Na+2H2O=2NaOH+H2↑ |
| B、2F2+2H2O=4HF+O2 |
| C、NaH+H2O=NaOH+H2↑( NaH中H为-1价) |
| D、Cl2+H2O=HCl+HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:
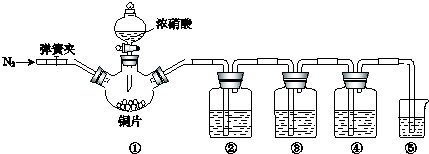
| 实验过程 | 实验现象 |
| Ⅰ.检验装置的气密性 | \ |
| Ⅱ.… | \ |
| Ⅲ.打开分液漏斗活塞,将浓硝酸缓慢滴入烧瓶中,关闭活塞. | ①中产生大量的红棕色气体,红棕色气体在②中变为无色,气体通过③后依然为无色,通过④后变为红棕色 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 操作 | 现象 | 结论 |
| 假设一不成立 |
查看答案和解析>>
科目:高中化学 来源: 题型:
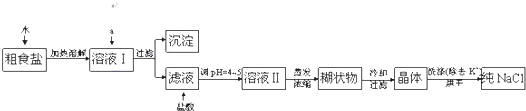
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、FeCl2溶液中通入Cl2 Fe2++Cl2═Fe3++2Cl- |
| B、Fe和稀硫酸反应 2Fe+6H+═2Fe3++3H2↑ |
| C、FeCl3溶液与铜 Fe3++Cu═Fe2++Cu2+ |
| D、用醋酸除水垢 2CH3COOH+CaCO3═2CH3COO-+Ca2++H2O+CO2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com