
 电渗析法是一种利用A、B离子交换膜进行海水淡化的方法,其原理如图所示.已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极.下列叙述中正确的是( )
电渗析法是一种利用A、B离子交换膜进行海水淡化的方法,其原理如图所示.已知海水中含Na+、Cl-、Ca2+、Mg2+、SO42-等离子,电极为惰性电极.下列叙述中正确的是( )| A. | 是原电池装置,把化学能转化为电能 | |
| B. | 是电解装置,只发生物理变化 | |
| C. | 左右池中得到淡水 | |
| D. | A膜是阴离子交换膜,B膜是阳离子交换膜 |
分析 A、是直流电源作用在两极分别发生氧化还原反应;
B、是电解池装置,将化学能转化为电能,两极分别发生氧化还原反应;
C、溶液中钠离子、钙离子和硫酸根离子,始终不放电;
D、阴离子交换膜只允许阴离子自由通过,阳离子交换膜只允许阳离子自由通过.
解答 解:A、是直流电源作用在两极分别发生氧化还原反应,电能转化为化学能,是电解池,故A错误;
B、是电解池装置,将化学能转化为电能,两极分别发生氧化还原反应,发生化学变化,故B错误;
C、溶液中钠离子、钙离子和硫酸根离子,始终不放电,所以得不到淡水,故C错误;
D、阴离子交换膜只允许阴离子自由通过,阳离子交换膜只允许阳离子自由通过,隔膜B和阴极相连,阴极是阳离子放电,所以隔膜B是阳离子交换膜,故D正确;
故选D.
点评 本题考查了电解原理的应用,电极反应,电极判断,题干信息的分析应用,题目难度中等.


 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
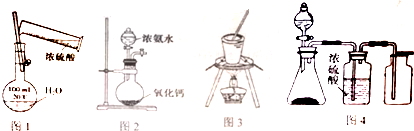
| A. | 用图1所示配制一定浓度的稀硫酸 | B. | 用图2装置实验室制取氨气 | ||
| C. | 用图3装置蒸发饱和食盐水 | D. | 用图4装置制取、收集乙炔气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 戊烷、戊醇、戊烯、乙酸乙酯中同分异构体数目最少的是戊烯 | |
| B. | 分子式为C5H12O且可与金属钠反应放出氢气的有机化合物有8种 | |
| C. | 将2-丙醇与NaOH的醇溶液共热可制备CH3-CH=CH2 | |
| D. |  三种氨基酸脱水,最多可生成6种二肽 三种氨基酸脱水,最多可生成6种二肽 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
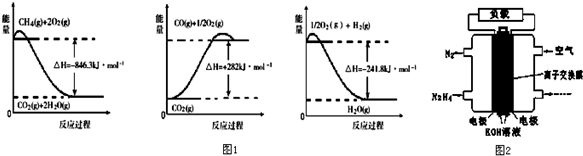
 (1)如图为1molNO2(g)和1molCO(g)反应生成NO(g)和CO2(g)过程中的能量变化示意图.已知E1=134KJ/mol,E2=368KJ/mol( E1、E2为反应的活化能).若在反应体系中加入催化剂,反应速率增大,则E1、△H的变化分别是减小、不变(填“增大”、“减小”或“不变”).写出该反应的热化学方程式NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ•mol-1.
(1)如图为1molNO2(g)和1molCO(g)反应生成NO(g)和CO2(g)过程中的能量变化示意图.已知E1=134KJ/mol,E2=368KJ/mol( E1、E2为反应的活化能).若在反应体系中加入催化剂,反应速率增大,则E1、△H的变化分别是减小、不变(填“增大”、“减小”或“不变”).写出该反应的热化学方程式NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJ•mol-1.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 自行车的钢圈上镀一层铬,防止生锈 | |
| B. | 外加直流电源保护钢闸门时,钢闸门与电源的负极相连 | |
| C. | 钢铁发生吸氧腐蚀的正极反应:2H2O+O2+4e-═4OH- | |
| D. | 钢铁发生析氢腐蚀的负极反应:Fe-3e-═Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 常温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol•L-1的NaOH溶液.整个实验进程中溶液的pH变化曲线如图所示,下列叙述正确的是( )
常温下,将Cl2缓慢通入水中至饱和,然后向所得饱和氯水中滴加0.1mol•L-1的NaOH溶液.整个实验进程中溶液的pH变化曲线如图所示,下列叙述正确的是( )| A. | 实验进程中可用pH试纸测定溶液的pH | |
| B. | 向a点所示溶液中通入SO2,溶液的酸性和漂白性均增强 | |
| C. | c点所示溶液中:c(Na+)=2c(ClO-)+c(HClO) | |
| D. | 由a点到b点的过程中,溶液中$\frac{c({H}^{+})}{c(CI{O}^{-})}$减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D | |
| 用途 | 热的纯碱溶液可去油污 | 明矾可用于净水 | 抗坏血酸(Vc)可作抗氧化剂 | 液氨可做制冷剂 |
| 解释 | 纯碱水解呈碱性 | 明矾在水中生成的氢氧化铝胶体有吸附性 | Vc具有酸性 | 液氨汽化时吸收大量的热 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
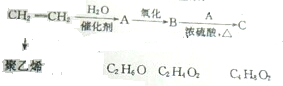
 ,该反应的单体为CH2=CH2,链节为-CH2-CH2-,聚合度为n.
,该反应的单体为CH2=CH2,链节为-CH2-CH2-,聚合度为n.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com