
| A. | 1:200 | B. | 200:1 | C. | 100:1 | D. | 1:100 |
分析 先根据水的离子积常数计算氢氧化钡溶液中c(OH-),盐酸中的c(H+),再得到pH=7的溶液,则n(H+)=n(OH-),根据n=cV计算氢氧化钡和盐酸的体积之比.
解答 解:将pH=9的Ba(OH)2溶液中c(OH-)=10-5mol/L,pH=3的稀盐酸中c(H+)=10-3mol/L,
设氢氧化钡的体积为x,盐酸的体积为y,欲使混合溶液pH=7,溶液呈中性,则n(H+)=n(OH-),则x•10-5mol/L=y•10-3mol/L,解得x:y=100:1,所以盐酸与Ba(OH)2溶液的体积比为1:100.
故选D.
点评 本题考查了离子积常数的有关计算,注意室温下题中混合溶液的pH=7时溶液呈中性,则n(H+)=n(OH-).


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题
 ;
; .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定有SO42- | B. | 一定有CO32- | ||
| C. | 不能确定Cl-是否存在 | D. | 不能确定SO42- 是否存在 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
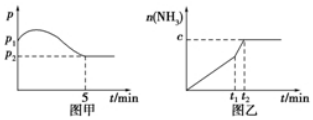
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 饱和Na2CO3溶液中BaSO4沉淀转化为BaCO3沉淀 | |
| B. | 升高温度,化学平衡发生移动是因为平衡常数改变 | |
| C. | 持续加热,水中MgCO3逐渐转化为更难溶的Mg(OH)2 | |
| D. | 改变一个影响因素使化学平衡发生移动,则平衡常数K值一定变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盖斯定律实质上是能量守恒定律的体现 | |
| B. | 在稀溶液中:H+(aq)+OH-(aq)═H2O(l)△H=-57.3 kJ/mol,含0.5mol H2SO4的浓硫酸与含1 mol NaOH的溶液混合,放出的热量大于57.3 kJ | |
| C. | 由C(石墨)→C(金刚石)△H=+73 kJ/mol,可知石墨比金刚石稳定 | |
| D. | 在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为:2H2(g)+O2(g)═2H2O(l)△H=-285.8 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 要求处理垃圾,但是又极力反对建造垃圾焚烧处理厂行为 | |
| B. | 夏天盖着被子吹空调 | |
| C. | 尽量购买本地的、当季的食物,减少食物的加工过程 | |
| D. | 开着5.6L排量的汽车直播声讨北京的雾霾天气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com