
| A、1mol 苯含有6nA个C-H键 |
| B、标准状况下,22.4L氨水含有nA个NH3分子 |
| C、18gH2O含有10nA个电子 |
| D、56g铁片投入足量浓H2SO4中生成nA个SO2分子 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 硫酸盐主要来自地层矿物质,多以硫酸钙、硫酸镁的形态存在.
硫酸盐主要来自地层矿物质,多以硫酸钙、硫酸镁的形态存在.| 温度(℃) | 527 | 758 | 927 |
| 平衡常数 | 784 | 1.0 | 0.04 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X元素的电子排布式为:1S22S22P63S23P63d104s24p64d65s2 |
| B、X元素位于第五周期 |
| C、X元素位于VIB族 |
| D、X元素原子最外层有2个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
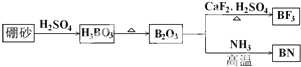
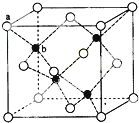
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
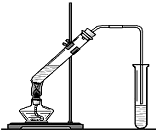 (1)装置中导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止
(1)装置中导管要插在饱和碳酸钠溶液的液面上,不能插入溶液中,目的是防止查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1 mol羟基(-OH)中含有的质子数为10 NA |
| B、相同状况下,22.4 L NO和11.2 L O2反应,生成物含有NA个分子 |
| C、在H2O2+Cl2=2HCl+O2反应中,每生成32 g氧气,则转移2 NA个电子 |
| D、1 mol Na2O2含有2 NA个阴离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
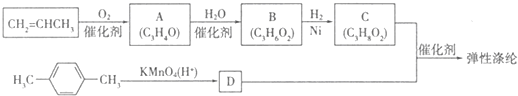
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com