
| 仪器 | 加入试剂 | 加入试剂的目的 |
| B | 饱和NaHCO3溶液 | |
| D | 吸收过量CO2 | |
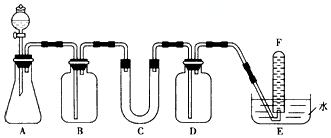
分析 由实验装置可知,本实验首先由CaCO3和盐酸反应生成CO2,氯化氢易挥发,制取的二氧化碳中含有氯化氢,产生气体通过饱和NaHCO3溶液,以除去CO2气体中混入的HCl,然后过氧化钠与CO2和水气反应,产生O2,用排水法收集O2,最后取出试管,立即把带火星的木条伸入试管口内,木条复燃,证明试管中收集的气体是氧气.
(1)碳酸的酸性弱于盐酸,实验室用碳酸钙和盐酸反应制取二氧化碳;
(2)Na2O2与CO2反应生成碳酸钠和氧气;
(3)A装置:制取二氧化碳,B装置:通过饱和的碳酸氢钠除去二氧化碳中的氯化氢,C装置:Na2O2与CO2反应,D装置:除去多余的二氧化碳,E装置:收集生成的气体氧气;
(4)根据氧气能支持燃烧确定检验氧气的方法.
解答 解:(1)A装置:盐酸的酸性强于碳酸,实验室通常使用石灰石或大理石(主要成分都为碳酸钙)与稀盐酸反应制取二氧化碳,碳酸钙与盐酸反应生成氯化钙、水和二氧化碳,反应方程式为CaCO3+2HCl═CaCl2+H2O+CO2↑,离子方程式为CaCO3+2H+=Ca2++H2O+CO2↑,
故答案为:CaCO3+2H+=Ca2++H2O+CO2↑;
(2)过氧化钠与二氧化碳反应生成碳酸钠和氧气,反应的方程式为:2Na2O2+2CO2═2Na2CO3+O2 ,
故答案为:2Na2O2+2CO2=2NaCO3+O2;
(3)A装置:利用碳酸钙与盐酸可以发生复分解反应生成氯化钙、水和二氧化碳的性质,制取二氧化碳,B装置:氯化氢易挥发,制取的二氧化碳中含有氯化氢,通过饱和的碳酸氢钠除去二氧化碳中的氯化氢,C装置:过氧化钠与CO2和水气反应,产生O2,D装置:用NaOH溶液洗气,吸收未反应的CO2气体,E装置:收集生成的气体氧气.
故答案为:除去CO2中的HCl;NaOH溶液;
(4)本实验的目的为证明过氧化钠可作供氧剂,收集气体后要验证是否为氧气,为防止倒吸,应先把E中的导管移出水面,然后关闭分液漏斗活塞,用拇指堵住试管口,取出试管,立即用带火星的木条伸到试管F的管口,如果木条复燃,说明过氧化钠与二氧化碳反应产生氧气,可做供氧剂,
故答案为:取出试管,将带火星的木条伸入试管内,若木条复燃,说明该气体是O2.
点评 本题考查过氧化钠的性质的实验设计,题目难度中等,解答本题注意把握实验原理和相关实验的基本操作,注意除杂的先后顺序和检验氧气的操作方法.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 所含离子 | Fe2+ | SO42- | H+ | M |
| 浓度(mol•L-1) | 1 | 1 | 2 | 2 |
| A. | Na+ | B. | Mg2+ | C. | Cl- | D. | CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1molH2O所含质子数为8NA | |
| B. | 1摩尔氦气所含的原子数为2NA | |
| C. | 在标准状况下1L水所含分子数为$\frac{1}{22.4}$NA | |
| D. | 0.5molaL与足量盐酸反应转移的电子数为1.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A | B | C | D |
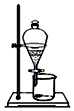 |  |  |  |
| 用酒精萃取碘水中的碘 | 烧杯中的Fe(OH)3胶体可产生丁达尔效应 | 蔗糖遇浓硫酸变黑,说明浓硫酸有脱水性 | Fe(OH)2白色沉淀迅速变成灰绿色,最后变成红褐色,说明Fe(OH)2易被氧化 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
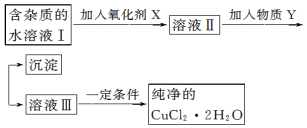
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的 pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀时的 pH | 3.0 | 9.0 | 6.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
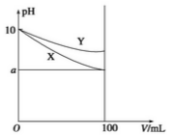 常温下,pH=10 的X、Y 两种碱溶液各1mL,分别稀释到100mL,其pH 与溶液体积(V)的关系如图所示,下列说法正确的是( )
常温下,pH=10 的X、Y 两种碱溶液各1mL,分别稀释到100mL,其pH 与溶液体积(V)的关系如图所示,下列说法正确的是( )| A. | 若8<a<10,则X、Y 都是弱碱 | |
| B. | 稀释后,X 溶液的碱性比Y 溶液的碱性强 | |
| C. | X、Y 两种碱溶液中溶质的物质的量浓度一定相等 | |
| D. | 分别完全中和X、Y 这两种碱溶液时,消耗同浓度盐酸的体积VX>VY |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com