
【题目】氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+ 2N2(g) ![]() Si3N4(s) + 6CO(g)
Si3N4(s) + 6CO(g)
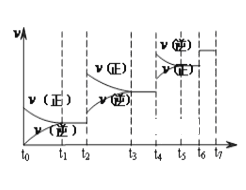
(1)达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率v与 时间t的关系如图。图中t4时引起平衡移动的条件可能是______________________;图中表示平衡混合物中CO的含量最高的一段时间是____________。
(2)若该反应的平衡常数为 K=729,则在同温度下1L密闭容器中,足量的SiO2和C与2mol N2充分反应,则N2的转化率是__________________ (提示:272 = 729)。
【答案】升高温度或增大压强t3~t450%
【解析】
(1)t4时正逆反应速率都较原平衡时的速率大,可升高温度或增大压强;t6时正逆反应速率都较原平衡时的速率大,但平衡不移动,前后气体系数之和不等,只能是使用催化剂;在t3~t4时反应向逆反应方向移动,则t3~t4时平衡混合物中CO的含量最高;因此,本题正确答案是:升高温度或缩小体积, t3~t4。
(2)设反应的氮气的物质的量为x,容器的体积为1L;
3SiO2(s)+ 2N2(g) +6C(s) ![]() 6CO(g) + Si3N4(s)
6CO(g) + Si3N4(s)
起始 2 0
转化 x 3x
平衡 2- x 3x
则平衡时氮气的浓度为(2-x)mol/L, CO的浓度为3xmol/L,则有:(3x)6/(2-x)2=729,解之得x=1,则氮气的转化率是1/2×100%=50%;正确答案:50%。


科目:高中化学 来源: 题型:
【题目】实验室里需要纯净的氯化钠溶液,但手边只有混有硫酸钠、碳酸氢铵的氯化钠。某学生设计了如下方案:
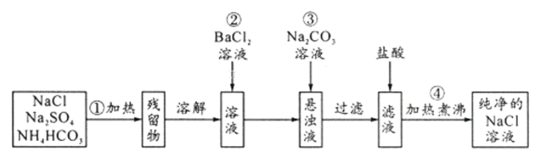
如果此方案正确,那么:
(1)操作①可选择________或________仪器。
(2)操作②是否可改为加硝酸钡溶液?为什么?________
(3)进行操作②后,如何判断SO42-已除尽,方法是__________________
(4)操作③的目的是__________,为什么不先过滤后加碳酸钠溶液?理由是___________。
(5)操作④的目的是________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测试一铁片中铁元素的含量,某课外活动小组提出下面两种方案并进行了实验(以下数据为多次平行实验测定结果的平均值):
方案一:将ag铁片完全溶解于过量稀硫酸中,测得生成氢气的体积为580 mL(标准状况);
方案二:将a/10g铁片完全溶解于过量稀硫酸中,将反应后得到的溶液用0.020 00 mol·L-1的KMnO4溶液滴定,达到终点时消耗了25.00 mL KMnO4溶液。
请回答下列问题:
(1)配平下面的化学方程式:__________________________
![]() KMnO4+
KMnO4+![]() FeSO4+
FeSO4+![]() H2SO4===
H2SO4===![]() Fe2(SO4)3+
Fe2(SO4)3+![]() MnSO4+
MnSO4+![]() K2SO4+
K2SO4+![]() H2O
H2O
(2)在滴定实验中不能选择________式滴定管,理由是______________;
(3)根据方案一和方案二测定的结果计算,铁片中铁的质量分数依次为________和________;
(4)若排除实验仪器和操作的影响因素,试对上述两种方案测定结果的准确性做出判断和分析。
①方案一________(填“准确”、“不准确”或“不一定准确”),理由是____________;
②方案二________(填“准确”、“不准确”或“不一定准确”),理由是_____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.铁是人体必需的微量元素,绿矾(FeSO4·7H2O)是治疗缺铁性贫血药品的重要成分。
(1)FeSO4溶液在空气中会因氧化变质产生红褐色沉淀,其发生反应的离子方程式是__________;实验室在配制FeSO4溶液时常加入____以防止其被氧化。请你设计一个实验证明FeSO4溶液是否被氧化__。
Ⅱ.硫酸亚铁铵[(NH4)2Fe(SO4)2·6H2O]较硫酸亚铁不易被氧气氧化,常用于代替硫酸亚铁。
(2)硫酸亚铁铵不易被氧化的原因是______________________。
(3)为检验分解产物的成分,设计如下实验装置进行实验,加热A中的硫酸亚铁铵至分解完全。

①A中固体充分加热较长时间后,通入氮气,目的是_____________________________。
②装置B中BaCl2溶液的作用是为了检验分解产物中是否有SO3气体生成,若含有该气体,观察到的现象为_。
③实验中,观察到C中有白色沉淀生成,则C中发生的反应为___________ (用离子方程式表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I. 某实验小组对H2O2的分解做了如下探究。下表是研究影响H2O2分解速率的因素时记录的一组数据,将质量相同但状态不同的MnO2分别加入盛有15 mL5%的H2O2溶液的大试管中,并用带火星的木条测试,结果如下:
MnO2 | 触摸试管情况 | 观察结果 | 反应完成所需的时间 |
粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 3.5min |
块状 | 微热 | 反应较慢,火星红亮,但木条未复燃 | 30min |
(1)该反应是_________反应(填放热或吸热)。
(2)实验结果表明,催化剂的催化效果与_____________________有关。
Ⅱ.某可逆反应在体积为5L的密闭容器中进行,在从0—3分钟各物质的物质的量变化情况如图所示(A、B、C均为气体)。
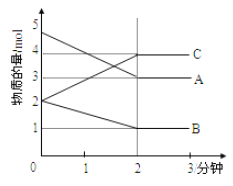
(3)该反应的的化学方程式为_____________。
(4)反应开始至2分钟时,B的平均反应速率为__________。
(5)能说明该反应已达到平衡状态的是_________。
A.v(A)= 2v(B) B.容器内压强保持不变
C.v逆(A)= v正(C) D.容器内混合气体的密度保持不变
(6)由图求得A的平衡时的转化率为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】右图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加几滴石蕊溶液。下列实验现象描述正确的是

A. 逸出气体的体积,a电极的小于b电极的
B. 一电极逸出无味气体,另一电极逸出刺激性气体
C. a电极附近呈红色,b电极附近呈蓝色
D. a电极附近呈蓝色,b电极附近呈红色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常见有机化合物转化关系如下图(部分反应条件已略去)。
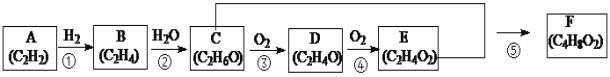
(1)A的结构式为_____;C中官能团的名称为_____;D物质的名称为_____。
(2)属于取代反应的有_____(填序号)。
(3)A光照生成G(分子式为C6H6),G分子中所有原子在同一平面,G既不能使酸性高锰酸钾溶液反应褪色,也不能使溴水反应褪色,则G的结构简式为_____。
(4)H是E的同分异构体,能发生水解反应,H的结构简式可能为_____。
(5)反应③的化学方程式为_____;反应⑤的化学方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上,合成氨反应N2 + 3H2 ![]() 2NH3的微观历程如下图所示。用
2NH3的微观历程如下图所示。用![]() 、
、![]() 、
、![]() 分别表示N2、H2、NH3,下列说法正确的是
分别表示N2、H2、NH3,下列说法正确的是
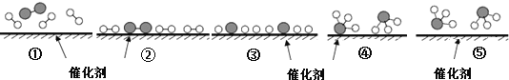
A. ①→② 催化剂在吸附N2、H2时,形成新的化学键
B. ②→③ 形成N原子和H原子是放热过程
C. ①→⑤ N2和H2全部化合成氨气
D. 使用合适的催化剂,能提高合成氨反应的效率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com