
【题目】下列关于元素周期表的叙述正确的是( )
A. 周期表中有八个主族,八个副族 B. 目前使用的元素周期表中,最长的周期含有32种元素
C. 短周期元素是指1-20号元素 D. 原子的最外层电子数都等于该元素所在的族序数
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A. 氯化钠中混有少量单质碘杂质,可用升华的方法提纯
B. 能使润湿的淀粉KI试纸变成蓝色的物质一定是Cl2
C. SO2可使酸性高锰酸钾溶液褪色,体现了SO2的漂白性
D. 浓硫酸具有吸水性,可以用作干燥剂,例如可用于NH3的干燥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验。
(1)若取ag样品,向其中加入足量的NaOH溶液,测得生成气体的体积(标准状况,下同)为b L 。反应的离子方程式为_______________________________________。样品中铝的质量为__________g。
(2)若使ag样品恰好完全反应,则反应中氧化铁与铝的质量比是_________,
化学方程式为___________________________________。
(3)待(2)中生成物冷却后,加入足量盐酸,测得生成的气体体积为c L ,该气体与(1)中所得气体的体积比c:b=____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 制取乙烯时,用CuSO4溶液除杂,也可改为NaOH溶液除杂
B. C2H4与C4H8一定属于同系物
C. 1mol 2-甲基-1-丁烯在标况体积约为22.4L
D. 石油催化重整可获得芳香烃
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,可逆反应A(g)+3B(g)![]() 2C(g) 达到平衡状态的标志是
2C(g) 达到平衡状态的标志是
A. 生成的速率与A分解的速率相等
B. 单位时间生成nmolA,同时生成3nmolB
C. A、B、C的浓度不再变化
D. A、B、C的分子数比为1:3:2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氨气是一种重要的化工原料,氨态氮肥是常用的肥料。
工业合成氨的化学方程式:N2 + 3H2![]() 2NH3+92.4KJ
2NH3+92.4KJ
(1)它是氮的固定的一种,属于_____________(选填“大气固氮”、“生物固氮” “人工固氮”);若升高温度,该平衡向____________方向移动(选填“正反应”或“逆反应”)。
(2)该反应达到平衡状态的标志是______________。(选填编号)
a.压强不变 b.v正(H2)= v正(NH3) c.c (N2)不变 d.c(NH3)= c(N2)
(3)欲使NH3产率增大,可采取的措施有_____________、____________。若容器容积为2L,开始加入的N2为0.1mol,20s后测得NH3的物质的量为0.08mol,则N2的平均反应速率为_________________________________________mol/(LS)。
(4)如下图所示,将集有氨气的试管倒置于水槽中,观察到试管内液面上升,溶液变为红色,解释发生该现象的原因____________________________________。

(5)(NH4)2SO4是常用的氮肥,长期施用时会使土壤酸化板结,
用离子方程式表示原因___________________________________
检验(NH4)2SO4含NH4+的方法是____________________。
____________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测定含有少量氯化钠小苏打(主要成分为NaHCO3)的含量有多种方法。
(1)用重量法。加热法样品,用化学方程式表示的反应原理是:____________________;
II.量气法:通过测得___________的体积,从而通过换算求得小苏打的含量。
(2)III.滴定法(容积法)反应原理:NaHCO3+HCl→NaCl+H2O+CO2↑,
NaHCO3呈弱碱性,故不宜用酚酞做指示剂,而常用__________作指示剂。用标准盐酸滴定样品,滴定终点时的现象是________________________
滴定法实验步骤如下图示

(3)“称量→溶解、定容”这两大步骤需要的仪器主要有:电子天平、药匙、100mL的容量瓶、___________、____________、___________等
(4)“取出20mL”使用的滴定管在水洗后没对其进行润洗,对滴定结果的影响是_______(“偏高”“偏低”“无影响”);必须“做二次实验”的理由__________________.
某化学兴趣小组的同学用重量法测定某品牌小苏打中NaHCO3的质量分数,进行了以下实验:称量样品置于烧杯中,向其中慢慢滴加稀盐酸,至不再产生气泡为止,测得的有关数据如下表所示。
物质 | 样品 | 消耗的稀盐酸 | 反应后的溶液 |
质量(g) | 4.5 g | 37.7 g | 40 g |
试计算:
(5)生成的质量CO2_________;样品中的NaHCO3的质量分数_______________(计算结果保留一位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二氢荆芥内酯(F)是有效的驱虫剂。其合成路线为:
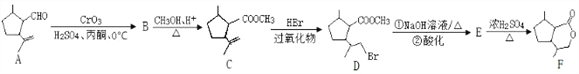
(1)B 的结构简式为__________________。
(2)C→D 的反应类型为___________。
(3)E 分子中的官能团名称为____________________________________。
(4)A 与新制氢氧化铜悬浊液反应的化学方程式_________________________。
(5)写出具有![]() 结构的 C 的一种同分异构体的结构简式___________________。
结构的 C 的一种同分异构体的结构简式___________________。
(6)写出由乙苯制取对溴苯乙烯(![]() )的合成路线。_________
)的合成路线。_________
(合成路线常用的表示方式为: ![]() )
)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com