
| A. | 从上至下,卤素单质的密度依次增大,碱金属单质的密度也依次增大 | |
| B. | 从上至下,卤素单质的沸点逐渐升高,碱金属单质的熔点逐渐降低 | |
| C. | 除了I2外,其它卤素单质都能将Fe氧化到+3价 | |
| D. | F2不能从NaCl溶液中置换出Cl2 |
分析 A、碱金属中钠的密度大于钾的密度;
B、卤素单质是分子晶体卤素单质的熔沸点随着原子半径增大而升高,碱金属单质的熔沸点逐渐降低;
C、卤素单质的氧化性从上到下逐渐减弱;
D、F2能和NaCl溶液中的水剧烈反应产生氧气.
解答 解:A、碱金属和卤素单质的密度都依次变大,但是钠钾反常,钠的密度大于钾的密度,故A错误;
B、卤素单质是分子晶体,分子晶体的熔沸点与其相对分子质量成正比,所以卤素单质的熔沸点随着原子半径增大而升高,碱金属单质的熔沸点逐渐降低,故B正确;
C、卤素单质的氧化性从上到下逐渐减弱,除了I2外,其它卤素单质都能将Fe氧化到+3价,故C正确;
D、F2能和NaCl溶液中的水剧烈反应产生氧气,不能从NaCl溶液中置换出氯气,故D正确.
故选A.
点评 本题以碱金属族、卤族元素为例考查同一主族元素性质递变规律,同时考查学生灵活运用知识能力,题目难度不大.


科目:高中化学 来源: 题型:解答题
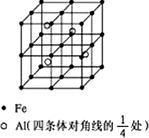 第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物.
第四周期过渡元素Fe、Ti可与C、H、N、O形成多种化合物.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 新制氯水中没有氯气分子 | |
| B. | 新制氯水在光照的条件下,可以产生气体,该气体是氯气 | |
| C. | 新制氯水中滴加硝酸银溶液,没有任何现象 | |
| D. | 新制氯水可以使干燥的布条褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | m>n | B. | m<n | C. | m=n | D. | 不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由分子构成的物质中一定含有共价键 | |
| B. | 形成共价键的元素不一定是非金属元素 | |
| C. | 正四面体结构的分子中的键角一定是109°28′ | |
| D. | ClO2-的空间构型为直线型 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com