
下列叙述不正确的是
A.植物油的不饱和程度高于动物油,植物油更易氧化变质
B.除去乙酸乙酯中少量的乙酸:用饱和碳酸钠溶液洗涤、分液
C.过氧化钠中含有离子键和非极性共价键,阴离子与阳离子的物质的量之比为1:1
D.向某溶液中滴入稀盐酸产生使澄清石灰水变浑浊的气体,该溶液不一定含有CO32-
科目:高中化学 来源:2014-2015黑龙江省高二上学期期末考试化学试卷(解析版) 题型:填空题
(14分)A、B代表不同物质,都是H、N、O、Na中的任意三种元素组成的强电解质,A的水溶液呈碱性,B的水溶液呈酸性,请找出A、B可能的两种组合。(要求:相同浓度时,A1溶液中水的电离程度小于A2溶液中水的电离程度;相同浓度时,B1溶液中水的电离程度小于B2溶液中水的电离程度.)
(1)写出化学式:A1________,A2________,B1________,B2________;
(2)相同温度下,当A1、B1的物质的量浓度相等时,两溶液中水电离出的氢离子的物质的量浓度之比为____________;常温下,若B1、B2两溶液的pH=5,则两溶液中由水电离出的氢离子的物质的量浓度之比为________;
(3)写出0.1 mol/L的A2溶液中离子浓度大小排序______________________________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年上海市十三校高三第二次联考化学试卷(解析版) 题型:选择题
足量铜溶于一定量浓硝酸,产生NO2、N2O4、NO的混合气体,这些气体若与1.12LO2(标准状况)混合后通入水中,气体被水完全吸收。若向原所得溶液中加入5 mol·L-1H2SO4溶液100 mL,则继续溶解的Cu的质量为
A.6.4g B.9.6g C.19.2g D.24g
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市顺义区高三第一次统一练习化学试卷(解析版) 题型:填空题
(14分)A是一种重要的食用香料。存在于玉米、葡萄等多种食品中。主要用于配制奶油、乳品、酸奶和草莓等香精,也可用于有机合成。以A为原料制备阴离子树脂M和新型聚酯材料N等的合成路线如下:
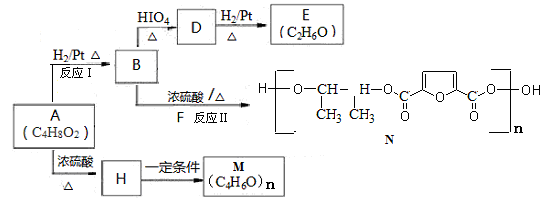
已知:Ⅰ.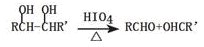
Ⅱ. 不稳定,很快转化为
不稳定,很快转化为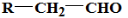
(1)反应Ⅰ的反应类型是 。
(2)B中官能团的名称是 。
(3)D与新制Cu(OH)2反应的化学方程式是 。
(4)下列关于E的说法正确的是 。
a.不溶于水 b.能与H2发生还原反应
c.能被重铬酸钾酸性溶液氧化 d.与NaOH醇溶液共热发生消去反应
(5)M的结构简式是 。
(6)反应Ⅱ的化学方程式是 。
(7)A的属于酯类的同分异构体有____种,其中只含一个甲基的同分异构的结构简式是: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市顺义区高三第一次统一练习化学试卷(解析版) 题型:选择题
某同学利用下图所示装置探究金属的腐蚀与防护条件。下列说法不合理的是

A.①区Cu电极上产生气泡,Fe电极附近滴加K3[Fe(CN)6]后出现蓝色,Fe被腐蚀
B.②区Cu电极附近滴加酚酞后变成红色,Fe电极附近滴加K3[Fe(CN)6]出现蓝色,Fe被腐蚀
C.③区Zn电极反应式为Zn-2e-===Zn2+,Fe电极附近滴加K3[Fe(CN)6]未出现蓝色,Fe被保护
D.④区Zn电极反应式为2H+ + 2e-===H2↑,Fe电极附近滴加K3[Fe(CN)6]出现蓝色, Fe被腐蚀
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市顺义区高三第一次统一练习化学试卷(解析版) 题型:选择题
化学与生产、生活、社会密切相关,下列说法不正确的是
A.明矾[KAl(SO4)2·12H2O]溶于水会形成胶体,因此可用于自来水的杀菌消毒
B.小苏打是制作面包等糕点的膨松剂,还是治疗胃酸过多的一种药剂
C.蛋白质、淀粉、油脂等都能在人体内水解并提供能量
D.纯净的二氧化硅是现代光学及光纤制品的基本原料
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省扬州市高三上学期期末考试化学试卷(解析版) 题型:实验题
(12分)氯化亚铜是一种应用较广的催化剂,易水解。以低品位铜矿砂(主要成分CuS)为原料制备氯化亚铜的路线如下:
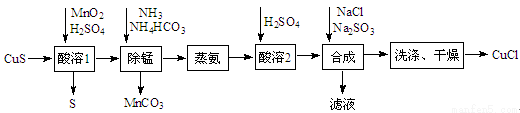
(1)酸溶1步骤中加入MnO2的作用是 。
(2)除锰步骤Mn2+转化为MnCO3沉淀,该反应的离子方程式为 。溶液中CuSO4转变为Cu(NH3)4CO3留在溶液中。
(3)蒸氨步骤会得到CuO固体,该步骤在减压条件下进行的原因是 。
(4)合成步骤加入Na2 SO3的速率不宜过快,否则会产生SO2气体,除可能与酸溶时硫
SO3的速率不宜过快,否则会产生SO2气体,除可能与酸溶时硫 酸过量有关,还可能的原因是 。
酸过量有关,还可能的原因是 。
(5)有工艺将合成步骤的NaCl与Na2SO3换为NH4Cl和(NH4)2SO3,则可获 得一种可作为氮肥的副产品,其化学式为 。
得一种可作为氮肥的副产品,其化学式为 。
(6)洗涤步骤先用 洗,再用无水乙醇洗涤。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年北京市通州区高三模拟考试(一)理综化学试卷(解析版) 题型:填空题
中国环境监测总站数据显示,PM2.5、SO2、NOx等是连续雾霾过程影响空气质量显著的污染物,其主要来源为燃煤、机动车尾气等。因此,对它们进行研究具有重要意义。请回答:
(1)将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
离子 | K+ | Na+ | NH | SO | NO | Cl- |
浓度(mol/L) | 4×106 | 6×106 | 2×105 | 4×105 | 3×105 | 2×105 |
根据表中数据计算PM2.5待测试样的pH = 。
(2)NOx是汽车尾气的主要污染物之一。汽车发动机工作时会引发N2和O2反应,其能量变化示意图如下:
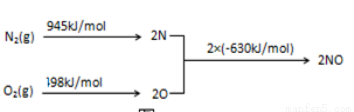
N2(g)+O2(g) 2NO(g) △H= 。
2NO(g) △H= 。
(3)消除氮氧化物和硫氧化物有多种方法。
Ⅰ.NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应原理如图所示:
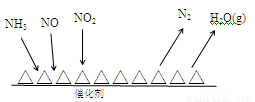
①由图可知SCR技术中的氧化剂为 。
②用Fe做催化剂时,在氨气足量的情况下,当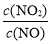 =1:1时,脱氮率最佳,已知每生成28g N2 放出的热量为QkJ,该反应的热化学方程式为 。
=1:1时,脱氮率最佳,已知每生成28g N2 放出的热量为QkJ,该反应的热化学方程式为 。
Ⅱ.工业上变“废”为宝,吸收工业中SO2和NO,可获得Na2S2O4和NH4NO3产品的流程图如下(Ce为铈元素):
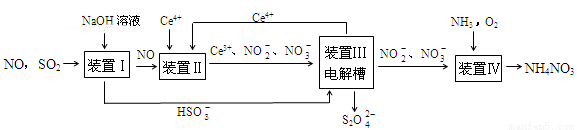
①装置Ⅰ中的主要反应的离子方程式为 。
②装置Ⅲ还可以使Ce4+再生,若用甲烷燃料电池电解该装置中的溶液,当消耗1mol CH4时,
理论上可再生 mol Ce4+。
Ⅲ.用活性炭还原法可以处理氮氧化物。如发生反应:
C(s)+2NO(g) N2(g)+CO2(g) △H=Q kJ/mol。
N2(g)+CO2(g) △H=Q kJ/mol。
在T1℃时,反应进行到不同时间测得各物质的浓度如下:
浓度(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①Tl℃时,该反应的平衡常数K= 。
②30 min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是________(答一种即可)。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年陕西省西安市高三下学期二模考试理综化学试卷(解析版) 题型:选择题
A、B、C、D、E五种短周期元素的原子序数依次增大,A和D,C和E分别同主族,E的原子序数为C的两倍,B的最外层电子数为A的最外层电子数的4倍。下列叙述正确的是
A.A、B、C三种元素形成的化合物一定是非电解质
B.A与C只能形成化学式为A2C的化合物
C.第三周期中,D的原子半径最大
D.E的氧化物对应的水化物一定具有强氧化性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com