
| A、1-溴丙烷与2-溴丙烷发生消去反应的产物不相同 |
| B、苯、甲苯在一定条件下均能发生取代反应 |
| C、通过红外光谱分析可以区分CH3CH2OH和CH3OCH3 |
D、异戊二烯(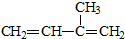 )与等物质的量的溴单质反应,产物只有一种 )与等物质的量的溴单质反应,产物只有一种 |


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:
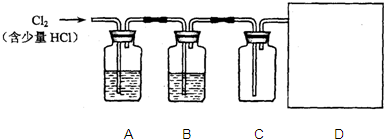
| 实验步骤 | 预期现象和相应结论 | |
| i |  试管B中的试剂为澄清石灰水.向试管A中滴入盐酸. 试管B中的试剂为澄清石灰水.向试管A中滴入盐酸. |
①若 ②若 |
| ii | 若“假设一”不成立,向实验步骤i反应后的试管A中滴入2滴 |
①若 中的②分析,则“假设三”成立. ②若 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在多电子的原子里,能量高的电子通常在离核近的区域内运动 |
| B、最外层电子数为8的微粒均是稀有气体元素的原子 |
| C、俄国化学家道尔顿为元素周期表的建立作出了巨大贡献 |
| D、在周期表中金属和非金属的分界线附近寻找制备半导体材料 |
查看答案和解析>>
科目:高中化学 来源: 题型:
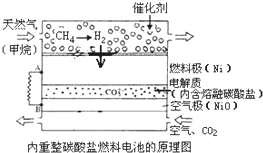 以熔融Li2CO3和K2CO3为电解质,天然气经内重整催化作用提供反应气的燃料电池如图,下列说法不正确的是( )
以熔融Li2CO3和K2CO3为电解质,天然气经内重整催化作用提供反应气的燃料电池如图,下列说法不正确的是( )| A、外电路电子流动方向:由A流向B |
| B、空气极发生反应的离子方程式是O2+4e-=2O2- |
| C、以此燃料电池为电源电解精炼铜,当电路有0.6mol e?转移,有19.2g精铜析出 |
| D、负极反应为H2-2e-+CO32-=CO2+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、装饰材料中的甲醛和芳香烃会造成居室污染 |
| B、石蜡油分解产生的气体不能使酸性高锰酸钾溶液褪色 |
| C、分子组成为CH2Cl2和C2H6O的有机物都存在同分异构现象 |
| D、油脂、葡萄糖、蛋白质都是人体重要的营养物质,它们都能发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
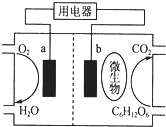 以葡萄糖为燃料的微生物燃料电池结构如图所示.a为电池的正极,关于该电池的叙述正确的是( )
以葡萄糖为燃料的微生物燃料电池结构如图所示.a为电池的正极,关于该电池的叙述正确的是( )| A、该电池能够在高温下工作 |
| B、b电极发生还原反应 |
| C、O2在a电极被氧化 |
| D、电流从a电极经用电器流向b电极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Fe与标准状况下2.24L Cl2恰好完全反应,转移电子数目为0.2NA |
| B、0.5mol Na2O2和0.5mol Na2O组成的混合物中,含阴离子数目为1.5NA |
| C、17g NH3分子中含有的共用电子对数为3NA |
| D、1.7g OH-所含电子总数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硫酸铜溶液与足量氢氧化钡溶液混合:Ba2++SO42-═BaSO4↓ |
| B、金属钾与水反应:K+2H2O═K++2OH-+H2↑ |
| C、碳酸氢钙溶液中加入少量氢氧化钠溶液:HCO3-+Ca2++OH-═CaCO3↓+H2O |
| D、次氯酸钙溶液中通入少量SO2气体:Ca2++2ClO-+SO2+H2O═2HClO+CaSO3↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:
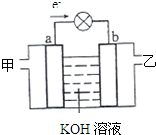 “水煤气(CO、H2)-空气”燃料电池的工作原理如图所示,其中a、b均
“水煤气(CO、H2)-空气”燃料电池的工作原理如图所示,其中a、b均| A、甲处通入的是空气,乙处通入的是水煤气 |
| B、a电极发生还原反应,b电极发生氧化反应 |
| C、用该电池电镀铜,若待镀金属增重6.4g,至少消耗标准状况下的水煤气2.24L |
| D、a电极的反应式包括:CO+4OH-+2e-═CO32-+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com