
 ���ڹ�������ũҵ����������Ҫ���ã�
���ڹ�������ũҵ����������Ҫ���ã�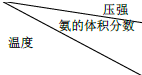 | 15.2MPa | 20.3MPa | 30.4MPa |
| 400�� | 32.8% | 38.8% | 48.2% |
| 450�� | 22.4% | 27.5% | 35.9% |
| 500�� | 14.9% | 18.8% | 25.8 |
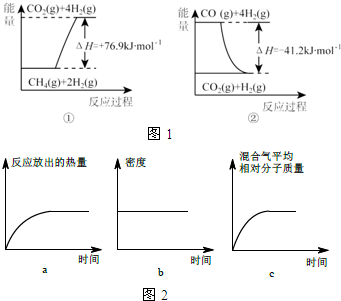
���� ��1����Ӧ�ٷ�Ӧ�����������������������ͣ�Ϊ���ȷ�Ӧ�����ݸ�˹���������㷴Ӧ���ʱ䲢��д�Ȼ�ѧ����ʽ��
�ڸ����¶Ⱥ�ѹǿ�Ի�ѧƽ���ƶ���Ӱ��֪ʶ���ش�
��I���ɱ����е����ݿ�֪���¶���ͬʱ��ѹǿԽ�����������Խ��ѹǿ��ͬʱ���¶�Խ�ߣ������������ԽС��
II��a��N2��H2����NH3һ��ʱ���Ӧ�ﵽƽ�⣻
B����Ӧ������������ܶȵ�����������ϵ����ı�ֵ��
c����ʼʱ��������ƽ����Է���������Ϊ0��
��� �⣺��1����Ӧ�ٷ�Ӧ�����������������������ͣ�Ϊ���ȷ�Ӧ����ͼʾ�ɵã�CH4��g��+2H2O��g��=CO2��g��+4H2��g����H=+76.9kJ/mol��CO��g��+H2O��g��=CO2��g��+H2��g����H=-41.2kJ/mol���ɸ�˹���ɵ�CH4��g��+H2O��g��=CO��g��+3H2��g����H=+118.1kJ/mol��
�ʴ�Ϊ�����ȣ�CH4��g��+H2O��g��=CO��g��+3H2��g����H=+118.1kJ/mol��
����ʹ��Һ��������ʹƽ�������ƶ�������Ӧ��ѹ�����£���ѡb��
��I���ɱ����е����ݿ�֪���¶���ͬʱ��ѹǿԽ�����������Խ��ѹǿ��ͬʱ���¶�Խ�ߣ������������ԽС���ʴ�Ϊ�������������ϳɰ��ķ�Ӧ����Ϊ���ȷ�Ӧ��������ϵѹǿ��С�ķ�Ӧ�������¶�ƽ�������ƶ�������ѹǿ��ƽ�������ƶ���
II��N2��H2����NH3Ϊ���ȷ�Ӧ��һ��ʱ���Ӧ�ﵽƽ�⣬a��ȷ��
�������غ㡢����̶������Է�Ӧ������������ܶ���ʼ���ձ��ֲ��䣬b��ȷ��
�������غ㡢��Ӧ����������ʵ�����С�����Դӿ�ʼ��ƽ�⣬��������ƽ����Է����������������䣬����ʼʱ��������ƽ����Է���������Ϊ0��c����
��ѡab��
���� ���⿼�黯ѧ��Ӧ����������˹���ɡ���ɳ����ԭ����֪ʶ��ע��֪ʶ�����Ӧ���ǹؼ���


 ͨ��ѧ��Ĭд����ϵ�д�
ͨ��ѧ��Ĭд����ϵ�д� ���ƽ̸�������ѡ����ĩ���100��ϵ�д�
���ƽ̸�������ѡ����ĩ���100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
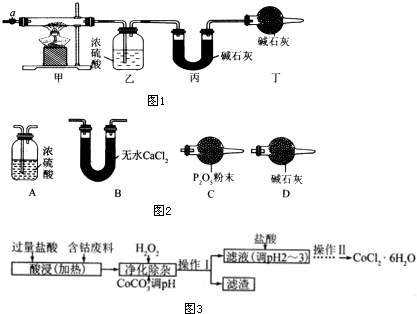
| ��װ�õ�����/g | ��װ�õ�����/g | |
| ����ǰ | 80.00 | 62.00 |
| ���Ⱥ� | 80.36 | 62.88 |
| ������ | Fe��OH��3 | Fe��OH��2 | Co��OH��2 | Al��OH��3 |
| ��ʼ������pH�� | 2.3 | 7.5 | 7.6 | 3.4 |
| ��ȫ������pH�� | 4.1 | 9.7 | 9.2 | 5.2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
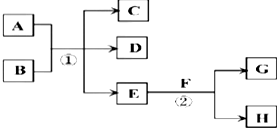
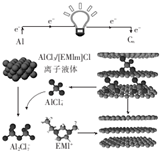 Ӣ������Ȼ�����ʽ��ڱ�����һ������ĭʯīϩ��CW����Ϊ�������ϵ����������ӵ�أ���ŵ�ʱ�Ĺ���ԭ����ͼ��ʾ������˵������ȷ���ǣ�������
Ӣ������Ȼ�����ʽ��ڱ�����һ������ĭʯīϩ��CW����Ϊ�������ϵ����������ӵ�أ���ŵ�ʱ�Ĺ���ԭ����ͼ��ʾ������˵������ȷ���ǣ�������| A�� | �ŵ�ʱ�������·��ת��1mol���ӣ�����������9g | |
| B�� | ���ʱ��ʯīϩ������ | |
| C�� | ���ʱ�������ĵ缫��ӦʽΪAlCl4-+3e-�TAl+4Cl- | |
| D�� | �ŵ�ʱ�������ĵ缫��ӦʽΪCW��AlCl4��+e-�TCW+AlCl4- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�Ӱ뾶��Na��Mg��Al | B�� | ���ȶ��ԣ�HCl��H2S��PH3 | ||
| C�� | ����ǿ����H2SiO3��H2CO3��H3PO4 | D�� | �۵㣺NaCl��Na��CO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
 ijѧ����0.2000mol•L-1�ı�NaOH��Һ�ζ�δ֪Ũ�ȵ����ᣬ������ɷ�Ϊ���¼�����
ijѧ����0.2000mol•L-1�ı�NaOH��Һ�ζ�δ֪Ũ�ȵ����ᣬ������ɷ�Ϊ���¼�����| �ζ����� | ���������ml�� | NaOH��Һ���������ml�� | |
| �ζ�ǰ | �ζ��� | ||
| 20.00 | 0.00 | 16.30 | |
| 2 | 20.00 | 0.00 | 16.22 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ij�¶��£�1L pH=8�Ĵ�ˮ�к�OH-Ϊ10 -6mol | |
| B�� | ��⾫��ͭ�����У����������ļ���ֵ����������������ֵһ����� | |
| C�� | �ϳɰ��ķ�Ӧ�Ƿ��ȷ�Ӧ������õ�������������߰����������� | |
| D�� | CH3COOH��Һ��ˮϡ�ͺ���Һ��$\frac{c��C{H}_{3}COOH��}{c��O{H}^{-}��}$��ֵ��С |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com