
����8�֣����ܱ������м����Ũ�ȵ�CO��H2O��T ��ʱ�������·�Ӧ��
CO(g) + H2O(g) ![]() CO2 + H2(g) ��H< 0
CO2 + H2(g) ��H< 0
��֪CO��Ũ�ȱ仯��ͼ��ʾ��

��1����0~4 min���÷�Ӧ��ƽ������v��CO��= mol/��L��min�����÷�
Ӧ��ƽ�ⳣ��Ϊ ��
��2��Ϊ������CO��ת���ʣ����Բ�ȡ�Ĵ�ʩ�� ��
a������Ӧ����CO��Ũ��
b�����ͷ�Ӧ�¶�
c�����ܱ��������ѹ����һ��
d���������˵Ĵ���
��3�������ı䷴Ӧ�¶Ⱥͷ�Ӧ����CO����ʼŨ�ȣ�ʹCO��ת���ʴﵽ90%����ˮ
��������ʼŨ������Ϊ ��
 ����ѧҵ���Ե�����ϵ�д�
����ѧҵ���Ե�����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����8�֣����ܱ������м����Ũ�ȵ�CO��H2O��T ��ʱ�������·�Ӧ��
CO(g) + H2O(g) CO2 + H2(g) ��H< 0
��֪CO��Ũ�ȱ仯��ͼ��ʾ��
��1����0~4 min���÷�Ӧ��ƽ������v��CO��= mol/��L��min�����÷�
Ӧ��ƽ�ⳣ��Ϊ ��
��2��Ϊ������CO��ת���ʣ����Բ�ȡ�Ĵ�ʩ�� ��
a������Ӧ����CO��Ũ��
b�����ͷ�Ӧ�¶�
c�����ܱ��������ѹ����һ��
d���������˵Ĵ���
��3�������ı䷴Ӧ�¶Ⱥͷ�Ӧ����CO����ʼŨ�ȣ�ʹCO��ת���ʴﵽ90%����ˮ
��������ʼŨ������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2011�콭�ո��ܸ��и�����һ���¿���ѧ�� ���ͣ������
����8�֣����ܱ������м����Ũ�ȵ�CO��H2O��T ��ʱ�������·�Ӧ��
CO(g) + H2O(g)  CO2 + H2(g) ��H< 0
CO2 + H2(g) ��H< 0
��֪CO��Ũ�ȱ仯��ͼ��ʾ��
��1����0~4 min���÷�Ӧ��ƽ������v��CO��= mol/��L��min�����÷�
Ӧ��ƽ�ⳣ��Ϊ ��
��2��Ϊ������CO��ת���ʣ����Բ�ȡ�Ĵ�ʩ�� ��
a������Ӧ����CO��Ũ��
b�����ͷ�Ӧ�¶�
c�����ܱ��������ѹ����һ��
d���������˵Ĵ���
��3�������ı䷴Ӧ�¶Ⱥͷ�Ӧ����CO����ʼŨ�ȣ�ʹCO��ת���ʴﵽ90%����ˮ
��������ʼŨ������Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�꽭��ʡ�ϲ��еڶ���ѧ�߶���һ���¿���ѧ�Ծ����������� ���ͣ�������
�����8�֣����ܱ������н���X2������+ 3Y2������ 2Z�������ķ�Ӧ����X2��Y2��Z����ʼŨ������Ϊ0.2mol/L��0.3mol/L��0.2mol/L������Ӧ��ƽ��ʱ��Ũ�ȷֱ���a��b��c��mol/L�����ش�
2Z�������ķ�Ӧ����X2��Y2��Z����ʼŨ������Ϊ0.2mol/L��0.3mol/L��0.2mol/L������Ӧ��ƽ��ʱ��Ũ�ȷֱ���a��b��c��mol/L�����ش�
�ٸ����ʵ�Ũ���п��ܵ��� ��
| A��c=0.5mol/L | B��b=0.5mol/L | C��c=0.4mol/L | D��a=0.3mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014�콭��ʡ�ϲ��и߶���һ���¿���ѧ�Ծ��������棩 ���ͣ�������
�����8�֣����ܱ������н���X2������+ 3Y2������ 2Z�������ķ�Ӧ����X2��Y2��Z����ʼŨ������Ϊ0.2mol/L��0.3mol/L��0.2mol/L������Ӧ��ƽ��ʱ��Ũ�ȷֱ���a��b��c��mol/L�����ش�
2Z�������ķ�Ӧ����X2��Y2��Z����ʼŨ������Ϊ0.2mol/L��0.3mol/L��0.2mol/L������Ӧ��ƽ��ʱ��Ũ�ȷֱ���a��b��c��mol/L�����ش�
�ٸ����ʵ�Ũ���п��ܵ��� ��
A��c=0.5mol/L B��b=0.5mol/L C��c=0.4mol/L D��a=0.3mol/L
����a= ʱ��b=0.15mol/L��
��a��b��ȡֵ���������һ�������� ��
��a��ȡֵ��Χ�ǣ� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2010-2011ѧ�꽭�ո��ܸ��и�����һ���¿���ѧ�� ���ͣ������
����8�֣����ܱ������м����Ũ�ȵ�CO��H2O��T ��ʱ�������·�Ӧ��
CO(g) + H2O(g)  CO2 + H2(g)
��H< 0
CO2 + H2(g)
��H< 0
��֪CO��Ũ�ȱ仯��ͼ��ʾ��
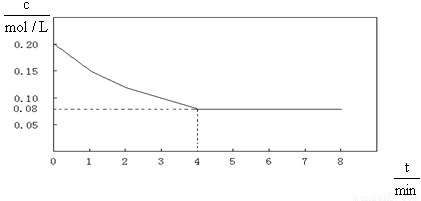
��1����0~4 min���÷�Ӧ��ƽ������v��CO��= mol/��L��min�����÷�
Ӧ��ƽ�ⳣ��Ϊ ��
��2��Ϊ������CO��ת���ʣ����Բ�ȡ�Ĵ�ʩ�� ��
a������Ӧ����CO��Ũ��
b�����ͷ�Ӧ�¶�
c�����ܱ��������ѹ����һ��
d���������˵Ĵ���
��3�������ı䷴Ӧ�¶Ⱥͷ�Ӧ����CO����ʼŨ�ȣ�ʹCO��ת���ʴﵽ90%����ˮ
��������ʼŨ������Ϊ ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com