
| A. | X的金属性比Y的金属性强 | |
| B. | 常温下,X和Y都不能从水中置换出氢 | |
| C. | Y元素的氢氧化物碱性比X 元素的氢氧化物碱性弱 | |
| D. | X元素的最高化合价比Y 元素的最高化合价高 |
分析 X和Y元素的原子,在化学反应中都容易失去电子而形成与Ne相同的电子层结构,说明两种金属原子核外有3个电子层,都为第三周期的金属元素,可能存在下列三种情况:Na和Mg,Na和Al,Mg和Al,结合同周期元素性质的递变规律和对应单质的可能性解答该题.
解答 解:X和Y元素的原子,在化学反应中都容易失去电子而形成与Ne相同的电子层结构,说明两种金属原子核外有3个电子层,都为第三周期的金属元素,可能存在下列三种情况:Na和Mg,Na和Al,Mg和Al,则
A.同周期元素的金属性从左到右逐渐减弱,X的核电荷数大,X的金属性小于Y,故A错误;
B.Y和X可能存在下列三种情况:Na和Mg,Na和Al,Mg和Al,而Na在常温下,易与水反应置换出氢气,故B错误;
C.金属性:Y>X,元素的金属性越强,则对应的最高价氧化物的水化物的碱性越强,则Y元素的氢氧化物碱性比X元素的氢氧化物碱性大,故C错误;
D.同周期元素从左到右元素的最外层电子数逐渐增多,X的核电荷数大,则X的最外层电子数多,最高化合价较Y的高,故D正确.
故选D.
点评 本题考查原子结构与元素周期律的关系,题目难度不大,注意根据失去电子而形成与Ne相同的电子层结构判断元素在周期表的中位置是解答该题的关键,学习中要把握元素周期律的递变规律.


 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案科目:高中化学 来源: 题型:实验题
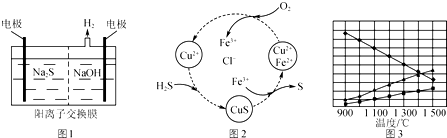
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL) | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Na+、HCO3-、NO3- | B. | Na+、SO42-、Cl-、S2- | ||
| C. | NH4+、Mg2+、SO42-、NO3- | D. | H+、K+、Na+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钠(固体) | B. | 少量硫酸铜溶液 | C. | Na2SO4溶液 | D. | 加热 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 含有大量Fe3+的溶液中:NH4+、Na+、Cl-、SCN- | |
| B. | 在强碱的溶液中:Na+、K+、ClO-、SO32- | |
| C. | 在强酸的溶液中:K+、Fe3+、Cl-、NO3- | |
| D. | 在强碱的溶液中:K+、Na+、Ca2+、HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com