
【题目】根据要求回答下列问题:
(1)在 ①液氯 ②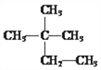 ③白磷 ④氯气
③白磷 ④氯气
⑤![]() ⑥
⑥![]() ⑦
⑦![]() ⑧红磷
⑧红磷
这八种物质中,互为同分异构体的是____,互为同素异形体的是_____。(填序号)
(2)在下列固体中:①CaCl2 ②KOH ③He ④H2SO4 ⑤NH4Cl ⑥金刚石
①其中不含化学键的晶体是_________,
②既含有离子键又含有共价键的物质是______,
③固体熔化时只需破坏共价键的晶体是____(填序号)
【答案】 ②和⑤ ③和⑧ ③ ②、⑤ ⑥
【解析】试题分析:(1)同分异构体是指分子式相同,但结构不同的化合物;
同素异形体是指由同种元素组成的不同单质;
(2)一般来说,活泼金属和活泼非金属元素之间易形成离子键,非金属元素之间易形成共价键,共价化合物中只含共价键,离子化合物中一定含有离子键,可能含有共价键,据此解答。
解析:(1)②与⑤分子式相同,结构不同,属于同分异构体;③与⑧是同种元素组成的不同单质,属同素异形体;
(2)①CaCl2含有离子键; ②KOH既含有离子键又含有共价键; ③He不含化学键; ④H2SO4 只含有共价键;⑤NH4Cl既含有离子键又含有共价键; ⑥金刚石只含有共价键。
①其中不含化学键的晶体是He;②既含有离子键又含有共价键的物质是KOH 、NH4Cl, ③固体熔化时只需破坏共价键的晶体是金刚石。


 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A. ![]() 的溶液中:Na+、K+、AlO2-、NO3-
的溶液中:Na+、K+、AlO2-、NO3-
B. 含有大量Fe3+的溶液中:NH4+、I-、Cl-、K+
C. pH=7的溶液中:NH4+、Al3+、SO42-、NO3-
D. 0.1mol·L-1Na2SO3的溶液中:H+、Ca2+、Fe2+、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知X、Y、Z、W为短周期主族元素,在周期表中的相对位置如图,有下列说法:
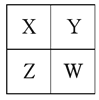
若HmXOn为强酸,则X的氢化物溶于水一定显酸性(m、n均为正整数)
若四种元素均为金属,则Z的最高价氧化物对应的水化物一定为强碱
若四种元素均为非金属,则W的最高价氧化物对应的水化物一定为强酸
④若四种元素只有一定为金属,则Z与Y的最高价氧化物对应的水化物一定为强酸。
其中不正确的说法有几项
A. 1项 B. 2项 C. 3项 D. 4项
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是

A. 图I装置中通入N2和O2的作用是相同的
B. 图Ⅱ中甲、乙两装置产生喷泉的原理一样
C. 图Ⅲ①装置中镁片是原电池的负极;②装置中镁片是原电池的正极
D. 图Ⅳ分液漏斗盛硝酸能证明非金属性N>C>Si,盛硫酸能证明非金属性S>C>Si
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F是短周期元素,周期表中A与B、B与C相邻;C与E同主族;A与C最外层电子数之比为2:3,B的最外层电子数比C的最外层电子数少1个; F元素的原子在周期表中半径最小;常见化合物D2C2与水反应生成C的单质,且溶液使酚酞溶液变红。
(1)E在周期表中的位置为____________________;B2F4的电子式_________________。
(2)B的最高价氧化物的水化物与其氢化物反应生成Z,则Z的名称为_______________,Z的化学键类型为____________________。
(3)可以比较C和E得电子能力强弱的是___________________(填写编号) 。
a.比较这两种元素最高正价的大小
b.二者形成的化合物中,D 元素的原子显负价
c.比较这两种元素的气态氢化物的稳定性
(4)两种均含C、D、E、F四种元素的化合物相互反应放出气体的反应离子方程式为_____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水煤气(CO 和H2)是合成甲醇的重要原料,它可用水蒸气通过炽热的炭层制得:C(s)+H2O(g)![]() CO(g)+H2(g) △H=+131.3kJ/mol
CO(g)+H2(g) △H=+131.3kJ/mol
⑴该反应的平衡常数的表达式为:_________________;升高温度,K值将 ;容器中气体的平均相对分子质量将 。(填“增大”、“减小”或“不变”)。
⑵上述反应达到平衡后,将体系中的C(s)部分移走,平衡将 (填序号)。
A.向左移 B.向右移 C.不移动
⑶下列事实能说明该反应在一定条件下已达到平衡状态的有 (填序号)。
A.单位体积内每消耗1molCO的同时生成1molH2
B.混合气体总物质的量保持不变
C.生成H2O(g)的速率与消耗CO的速率相等
D.H2O(g)、CO、H2的浓度相等
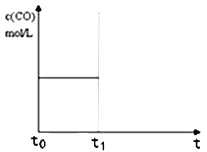
⑷上述反应在t0时刻达到平衡(如图),若在t1时刻改变某一条件,请在图中继续画出t1时刻后c(CO)随时间的变化曲线:
①缩小容器体积(用实线表示)。
②降低温度(用虚线表示)。
⑸某温度下,将4.0mol H2O(g)和足量的炭充入2L的密闭容器中,发生如下反应,C(s)+H2O(g)![]() CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为 。
CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示物质或微粒的化学用语或模型正确的是
A. 中子数为8的碳原子: ![]() B. S2-的结构示意图:
B. S2-的结构示意图: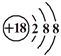
C. 二氧化碳电子式:![]() D. 氮气的结构式:N-N
D. 氮气的结构式:N-N
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验方法能达到实验目的的是
A.用淀粉溶液检验溶液中是否存在碘单质 B.用分液漏斗分离水与乙醇的混合物
C.用氯化钡溶液鉴别碳酸钠溶液与硫酸钠溶液 D.用排水集气法收集氯气
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com