
【题目】常温下氨气能被氯气氧化成N2,化工厂常用浓氨水检验管道是否泄漏氯气。某兴趣小组在实验室对氨气与氯气反应进行了探究,回答下列问题:
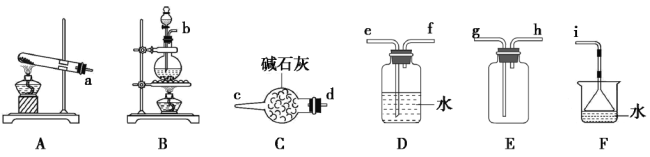
(1)氯气的发生装置可以选择上图中的_________(填大写字母),反应的离子方程式为________________。
(2)欲收集一瓶干燥的氨气,选择上图中的装置,其连接顺序为:发生装置→________(按气流方向,用小写字母表示)。
II.氯气与氨气的反应
室温下,用收集到的氯气与氨气按下图所示装进行实验(实验前K1、K2关闭)。

(3)为使两种气体充分混合,气体a是___________(填化学式)。
(4)
操作步骤 | 实验现象 | 解释原因 |
打开K1,缓缓推动注射器活塞,向试 管中注入气体a (约是气体b的3倍), 关闭K1,恢复室温 | 试管内出现白烟并在 试管内壁凝结 | ①反应的化学方程式________ |
打开K2 | ②_________ | ③_________ |
【答案】 B MnO2+2Cl-+4H+![]() Mn2++Cl2↑+2H2O d→c→h→g(→d→c)→i NH3 8NH3+3Cl2=N2+6NH4Cl 烧杯中的水倒吸入试管中 该反应是气体体积减小的反应,装置内压强降低,在大气压的作用下发生倒吸
Mn2++Cl2↑+2H2O d→c→h→g(→d→c)→i NH3 8NH3+3Cl2=N2+6NH4Cl 烧杯中的水倒吸入试管中 该反应是气体体积减小的反应,装置内压强降低,在大气压的作用下发生倒吸
【解析】 (1)实验室制备氯气是利用二氧化锰和浓盐酸加热反应生成氯气,反应类型是固体+液体![]() 气体,据此选择装置即写出反应的离子方程式;
气体,据此选择装置即写出反应的离子方程式;
(2)氨气是比空气轻的易溶于水的气体,制备得到氨气中含水蒸气,需要先通过碱石灰干燥后收集,剩余氨气需要吸收,吸收装置需要防止倒吸;
(3)氯气具有氧化性能氧化氨气生成氮气和氯化氢,氯化氢和过量氨气反应生成白色烟氯化铵固体小颗粒;
(4)打开K1,缓缓推动注射器活塞,向试管中注入约3倍于b气体的a气体,要求氨气过量,则a气体氨气,氨气极易溶于水分析。
详解:(1) 实验室利用二氧化锰和浓盐酸加热反应制备氯气,氯气的发生装置可以选择上图中的B,反应的离子方程式为MnO2+2Cl-+4H+![]() Mn2++Cl2↑+2H2O。
Mn2++Cl2↑+2H2O。
因此,本题正确答案是:B ;MnO2+2Cl-+4H+![]() Mn2++Cl2↑+2H2O;
Mn2++Cl2↑+2H2O;
(2)欲收集一瓶干燥的氨气,选择上图中的装置,按气流方向写出其接口的连接顺序:发生装置管口连装置C干燥氨气,收集气体导气管短进长出,剩余氨气可以通过装置(C后)被装置F中水吸收,发生装置管口d→c→h→g(→d→c)→i,
因此,本题正确答案是:d→c→h→g(→d→c)→i;
(3) 打开K1,缓缓推动注射器活塞,向试管中注入约3倍于b气体的a气体,根据现象分析氨气过量,则a气体氨气;关闭K1,恢复室温,试管中可观察到的现象是:生成白烟,而后凝结在试管内壁,发生反应的化学方程式为:8NH3+3Cl2=N2+6NH4Cl,
因此,本题正确答案是:NH3 ;8NH3+3Cl2=N2+6NH4Cl ;
(4)关闭K1,再打开打开K2,可观察到的现象是:烧杯中的水倒流进入试管中,原因是:该反应是气体体积减小的反应,装置内压强降低,在大气压的作用下发生倒吸,
因此,本题正确答案是:烧杯中的水倒流进入试管中;该反应是气体体积减小的反应,装置内压强降低,在大气压的作用下发生倒吸。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】已知:CO2(g)+3H2(g)CH3OH(g)+H2O(g)△H 现在体积为1L的密闭容器中,充入CO2和H2 . 实验测得反应体系中物质的物质的量与时间关系如下表,
n(CO2) | n(H2) | n(CH3OH(g) | n(H2O(g) | |
0 | 1.00mol | 3.25mol | 0.00 | 0.00 |
5min | 0.50mol | 0.50mol | ||
10min | 0.25mol | 0.75mol | ||
15min | 0.25mol | n1 |
回答下列问题:
(1)表格中的n1=
(2)0﹣5min内 v (H2)=
(3)该条件下CO2的平衡转化率为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2RO3是一种二元酸,常温下,用1Llmol/LNa2RO3溶液吸收RO2气体,溶液的pH随RO2气体的物质的量的变化如图所示。下列说法不正确的是
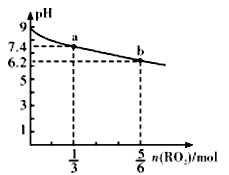
A. a点溶液中2c(Na+)>3c(RO32-)
B. 向b点溶液中加水可使溶液的pH由6.2升高到7.4
C. 常温下,NaHRO3溶液中c(HRO3-)>c(RO32-)>c(H2RO3)
D. 当吸收RO2的溶液呈中性时,c(Na+)=2c(RO32-)+c(HRO3-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某草酸晶体的化学式可表示为H2C2O4xH2O,为测定x的值,进行下列实验: ①称取7.56g某草酸晶体配成100.0mL的水溶液,
②用移液管移取25.00mL所配溶液置于锥形瓶中,加入适量稀H2SO4 , 用浓度为0.600mol/L的KMnO4溶液滴定,滴定终点时消耗KMnO4 的体积为10.00mL.
(1)若滴定终点时仰视读数,则所测x的值将(填“偏大”或“偏小”).
(2)x= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上采用乙苯与CO2脱氢生产重要化工原料苯乙烯  (g)+CO2(g)
(g)+CO2(g) 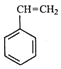 (g)=CO(g)+H2O(g)△H,其中乙苯在CO2气氛中的反应可分两步进行 A.
(g)=CO(g)+H2O(g)△H,其中乙苯在CO2气氛中的反应可分两步进行 A.  (g)
(g)  (g)+H2(g)△H1=﹣125KJ/mol
(g)+H2(g)△H1=﹣125KJ/mol
B.H2(g)+CO2(g)CO(g)+H2O(g)△H2=﹣41KJ/mol
(1)上述乙苯与CO2反应的反应热△H为
(2)苯乙烯与HCl加成的产物中具有手性异构体的分子的结构简式为 .
(3)在3L密闭容器内,乙苯与CO2的反应在三种不同的条件下进行实验,乙苯、CO2的起始浓度分别为1.0mol/L和3.0mol/L,其中实验I在T1℃,0.3MPa,而实验II、III分别改变了实验其他条件;乙苯的浓度随时间的变化如图I所示. 
①实验I乙苯在0﹣50min时的反应速率为
②实验Ⅱ可能改变条件的是
③图II是实验I中苯乙烯体积分数V%随时间t的变化曲线,请在图II中补画实验Ⅲ中苯乙烯体积分数V%随时间t的变化曲线.
(4)25℃时,将体积为Va PH=a的某一元强碱与体积为Vb PH=b的某二元强酸混合.若所得混合溶液的pH=11,且a=13,b=2,则Va:Vb= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下S2Cl2是橙黄色液体,其分子结构如图所示.少量泄漏会产生窒息性气味,遇水易水解,并产生酸性悬浊液.下列关于S2Cl2的说法错误的是( ) 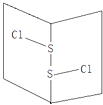
A.为非极性分子
B.分子中既含有极性键又含有非极性键
C.与S2Br2结构相似,熔沸点S2Br2>S2Cl2
D.与水反应的化学方程式可能为2S2Cl2+2H2O→SO2↑+3S↓+4HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期的三种元素X、Y、Z,原子序数依次变小,原子核外电子层数之和是5.X元素原子最外电子层上的电子数是Y和Z两元素原子最外电子层上的电子数的总和;Y元素原子的最外电子层上的电子数是它的电子层数的2倍,X和Z可以形成XZ3的化合物.请回答:
(1)X元素的名称是;Y元素的名称是;Z元素的名称是 .
(2)XZ3化合物的电子式是 .
(3)分别写出X、Y的含氧酸的分子式、 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期p区元素共有13种,除铝外全部是非金属元素。
(1)基态氮原子的价层电子排布图为_______________;短周期p区元素中,第一电离能最小的元素与电负性最大的元素组成的化合物是_______________(填化学式)。
(2)卤素与硼、氮、磷可形成BF3,NCl3和PBr3。下列有关以上三种分子的叙述正确的是_________;
A.化学键类型相同 B.空间构型相同
C.中心原子的杂化轨道类型相同 D.中心原子的价层电子对数相同
(3)CS2是一种溶剂,它能溶解硫磺。写出一种与CS2具有相同空间构型和键合形式的分子或离子______________。CO能与Ni形成正四面体型的配合物Ni(CO)4,3.42gNi(CO)4中含有_____molσ键。
(4)CCl4与水互不相溶,SiCl4与CCl4分子结构相似,但遇水极易发生水解反应,导致二者性质不同的原因是________________。
(5)铝的几种卤化物的熔点如下:
卤化铝 | AlF3 | AlCl3 | AlBr3 | AlI3 |
熔点/℃ | 1040 | 190 | 97.5 | 191 |
AlBr3的晶体类型是______,AlI3晶体中存在的作用力有_______________。
(6)氮化铝晶体为原子品体,是一种新型无机非金属材料,其晶体密度为ɑg/cm3,晶胞如图所示。
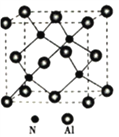
①铝原子的配位数为_______________。
②设NA为阿伏加德罗常数的值。氮化铝晶胞中,铝原子和氮原子之间最短的核间距为________nm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中的曲线是表示其他条件一定时,2NO(g)+O2(g) ![]() 2NO2(g) ΔH<0反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是( )
2NO2(g) ΔH<0反应中NO的转化率与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且v(正)>v(逆)的点是( )
A.a点
B.b点
C.c点
D.d点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com