
 .
.分析 (1)与氯元素同族的短周期元素为F,原子序数为9,核外电子数为9;
(2)上述转化过程中所涉及的短周期元素有O、Cl、Na,电子层越多,原子半径越大,同周期从左向右原子半径减小;
(3)利用单质之间的置换反应比较非金属性;CS2分子与CO2分子结构相似;
(4)电解氯化钠溶液可以得到NaClO3与H2,由电子、原子守恒可知反应为NaCl+3H2O$\frac{\underline{\;电解\;}}{\;}$NaClO3+3H2↑,该反应中Cl失去电子,H得到电子,共转移6e-;
(5)发生复分解反应,析出KClO3晶体,与其溶解度小有关.
解答 解:(1)与氯元素同族的短周期元素为F,原子序数为9,核外电子数为9,则核外电子排布式为1s22s22p5,故答案为:1s22s22p5;
(2)上述转化过程中所涉及的短周期元素有O、Cl、Na,电子层越多,原子半径越大,同周期从左向右原子半径减小,则原子半径由大到小的顺序是 Na>Cl>O,
故答案为:Na>Cl>O;
(3)利用单质之间的置换反应比较非金属性,能比较硫和氯非金属性强弱的化学反应方程式如H2S+Cl2=S+2HCl;CS2分子与CO2分子结构相似,CS2分子的结构式为S=C=S,
故答案为:H2S+Cl2=S+2HCl;S=C=S;
(4)电解氯化钠溶液可以得到NaClO3与H2,由电子、原子守恒可知反应为NaCl+3H2O$\frac{\underline{\;电解\;}}{\;}$NaClO3+3H2↑,该反应中Cl失去电子,H得到电子,共转移6e-,反应及电子转移的方向和数目为 ,
,
故答案为: ;
;
(5)II中不断加入细粒状KCl,搅拌,发生复分解反应,析出KClO3晶体.该反应能够发生的原因是室温下,氯酸钾在水中的溶解度明显小于其他晶体,
故答案为:室温下,氯酸钾在水中的溶解度明显小于其他晶体.
点评 本题考查原子结构与元素周期律,为高频考点,把握电子排布规律、元素周期律、氧化还原反应及溶解度等为解答的关键,侧重分析与应用能力的考查,综合性较强,题目难度不大.


 灵星计算小达人系列答案
灵星计算小达人系列答案 孟建平错题本系列答案
孟建平错题本系列答案科目:高中化学 来源: 题型:选择题
| A. |  用如图所示装置分离沸点相差较大的互溶液体混合物 | |
| B. |  用如图所示装置除去NaCO3固体中混有的NaHCO3 | |
| C. |  用如图所示装置除去Cl2中含有的HCl | |
| D. |  用如图所示装置进行电解法制离Cl2和H2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
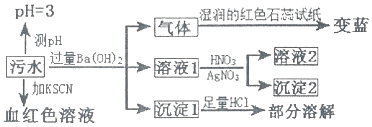
| A. | 该污水中一定存在Fe3+,不存在Fe2+ | |
| B. | 沉淀l为BaCO3和BaSO4 | |
| C. | 沉淀2可能为AgCl和Ag2SO4 | |
| D. | 该污水中一定存在NH4+、Cl-、Fe3+、SO42-离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 糖类、油脂和蛋白质在一定条件下一定都能水解 | |
| B. | 除去乙醇中的乙酸用分液的方法 | |
| C. | C5H10O2能与NaHCO3反应的结构有4种 | |
| D. | C8H10的同分异构体有三种,它们的性质相似 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验操作 | 现象 | 结论 | |
| A | 向25mL沸水中滴加5~6滴 FeCl3饱和溶液,持续加热煮沸 | 变为红褐色 | 最终制得 Fe(OH)3 胶体 |
| B | 欲收集酯化反应生成的乙酸乙酯并分离提纯,将导管伸入饱和Na2CO3溶液的液面下,再用分液漏斗分离 | 溶液分层,上层为无色油状液体 | 乙酸乙酯不溶于饱和Na2CO3 溶液,且密度比水小 |
| C | 淀粉溶液中加入几滴稀硫酸,水浴加热几分钟,再加入新制银氨溶液,水浴加热 | 无明显现象 | 淀粉未发生水解 |
| D | 两支盛有KI3溶液的向试管中,分别滴加淀粉溶液和AgNO3溶液 | 前者溶液变蓝,后者有黄色沉淀 | KI3溶液中存在平衡: I3-?I2+I- |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| 选项 | 实验操作和现象 | 结论 |
| A | 将Fe(NO3)2样品溶于稀H2SO4,溶液呈黄色. | Fe(NO3)2样品已被氧化变质 |
| B | 室温下,向 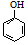 浊液中滴加Na2CO3溶液,浊液变澄清. 浊液中滴加Na2CO3溶液,浊液变澄清. | CO32-结合H+的能力比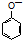 的强 的强 |
| C | 向Na2SiO3溶液中滴加稀硫酸,出现白色胶状沉淀. | 非金属性:S>Si |
| D | 向BaSO4中加入饱和Na2CO3溶液,充分搅拌,静置,过滤,洗涤.向滤渣中加盐酸,有气泡产生. | Ksp(BaCO3)<Ksp(BaSO4) |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙二醇与丙三醇互为同系物 | B. | 乙烯和丙烯具有相似的化学性质 | ||
| C. | 淀粉和纤维素属于同分异构体 | D. | 乙酸与甲酸甲酯均易溶于水 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
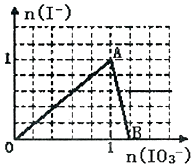 在含3molNaHSO3的溶液中加入含a mol NaIO3的溶液充分反应(不考虑I2+I-?I3-),所得溶液中的I-与加入NaIO3的物质的量的关系曲线如图所示,下列说法不正确的是( )
在含3molNaHSO3的溶液中加入含a mol NaIO3的溶液充分反应(不考虑I2+I-?I3-),所得溶液中的I-与加入NaIO3的物质的量的关系曲线如图所示,下列说法不正确的是( )| A. | 还原性HSO3->I-,氧化性:IO3->SO42->I2 | |
| B. | 当a=1时,溶液中n(I2):n(I-)=3:5 | |
| C. | AB段,反应的离子方程式为:IO3-+5I-+6H+═3I2+3H2O | |
| D. | l<a<1.2时,溶液中SO42-与I-的物质的量之比为3:(6-5a) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气溶于水形成纯净物-----氯水 | |
| B. | 实验室制取氯气后可以用向上排空气法收集 | |
| C. | 有氯气参与的反应可以用石灰乳做尾气处理 | |
| D. | 氧化性和毒性都属于氯气的化学性质 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com