
| A、Na+ 1s22s22p6 |
| B、O2- 1s22s22p6 |
| C、Si 1s22s22p2 |
| D、Al 1s22s22p63s23p1 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
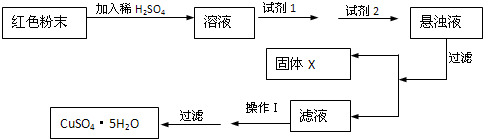
| 物质 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
| 开始沉淀pH | 6.0 | 7.5 | 1.4 |
| 沉淀完全pH | 13 | 14 | 3.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.8mol |
| B、1mol |
| C、1.5mol |
| D、2mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在有盐桥构成的铜-锌-稀硫酸原电池中,盐桥中的阳离子移向电池的锌极 |
| B、化学平衡的建立与途径无关,可以从正反应方向建立,也可以从逆反应方向建立 |
| C、可以借助分光度计采用比色的方法测定某反应的化学反应速率 |
| D、在FeCl3与过量的KI溶液充分反应后的溶液用CCl4萃取后,往上层溶液中加入几滴KSCN溶液,溶液出现血红色,说明该化学反应存在限度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
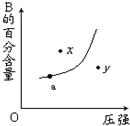 对于mA(s)+nB(g)?pC(g)△H<0的可逆反应,在一定温度下B的百分含量与压强的关系如图所示,则下列判断正确的是( )
对于mA(s)+nB(g)?pC(g)△H<0的可逆反应,在一定温度下B的百分含量与压强的关系如图所示,则下列判断正确的是( )| A、m+n<p |
| B、n<p |
| C、a点时增加A的物质的量,B的百分含量减小 |
| D、x点的状态是v正>v逆 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、v(D)=0.6 mol?L-1?min-1 |
| B、v(A)=0.2 mol?L-1?s-1 |
| C、v(C)=0.40 mol?L-1?min-1 |
| D、v(B)=0.45 mol?L-1?s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| pH | [H2CrO4] | [HCrO4-] | [CrO42-] | [Cr2O72-] |
| 4 | 0 | 0.095 | 0.035 | 0.435 |
| 7 | 0 | 0.086 | 0.274 | 0.320 |
| 10 | 0 | 0.004 | 0.990 | 0.003 |
| A、铬酸的电离方程式为H2CrO4═2H++CrO42- |
| B、铬酸的总浓度为1mol/L |
| C、[H+]越大,HCrO4-浓度越大 |
| D、已知Cr2O72-为橙色离子,CrO42-为黄色离子,随着pH的升高溶液将逐渐变为黄色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③ | B、③④ | C、①④ | D、②④ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com