




 ,
, ;
; ,M的最高价氧化物对应水化物的化学式为H2SO4,
,M的最高价氧化物对应水化物的化学式为H2SO4, ;H2SO4;
;H2SO4;| 30g |
| 14g/mol |
| 70g |
| 32g/mol |


 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
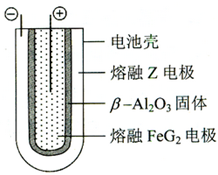 (2012?天津)X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大.X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子.
(2012?天津)X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大.X、Z同主族,可形成离子化合物ZX;Y、M同主族,可形成MY2、MY3两种分子.

| 充电 | 放电 |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源:2012-2013学年河南省许昌市六校高一第六次联考化学试卷(带解析) 题型:推断题
X、Y、Z、M、G五种元素分属三个短周期,且原子序数依次增大。X、Z同主
族,可形成离子化合物ZX,Y、M同主族,可形成MY2、MY3两种分子。请回答下列问题:
(1)Y在元素周期表中的位置为 。
(2)上述元素的最高价氧化物对应的水化物酸性最强的是 (写化学式),
非金属气态氢化物还原性最强的是 (写化学式)。
(3)X2M的燃烧热△H=-a kJ·mol-1,写出X2M燃烧反应的热化学方程式: 。
(4)ZX的电子式为 ;ZX与水反应放出气体的化学方程式为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com