
【题目】草酸晶体的组成可表示为H2C2O4·xH2O,为测定x值,进行下述实验:
实验1:准确称取Wg草酸晶体配成100ml水溶液;
实验2:用浓度为0.100molL-1KMnO4溶液滴定所配制的草酸溶液,所发生的反应为:2KMnO4+5H2C2O4+3H2SO4=K2SO4+ 10CO2↑+2MnSO4+8H2O。
试回答下列问题:
(1)实验1中,配制100ml草酸水溶液所需要的一组仪器是________(填相应编号)
A、0.001g的电子天平 B、50ml酸式滴定管 C、100ml量筒 D、100ml容量瓶 E、烧杯 F、胶头滴管 G、锥形瓶
(2)实验2中H2C2O4·xH2O中x值的测定是利用氧化还原反应滴定法
①其中正确操作步骤的顺序为___________
a.用移液管取用25.00ml所配的草酸溶液置于锥形瓶中,加适量的稀硫酸。
b.把盛有KMnO4标准液的滴定管固定好,调节滴定管尖嘴使之充满液体
c.取KMnO4标准液注入滴定管中至“0”刻度以上
d.调节液面至“0”或“0”刻度以下,记下读数
e.把标准KMnO4溶液润洗滴定管2~3次
f.把锥形瓶放在滴定管下面,用KMnO4标准液滴定至终点并记下滴定管的读数
②下列关于滴定分析,正确的是________________。
A. 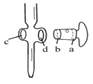 图中,应将凡士林涂在旋塞的a端和旋塞套内的c端
图中,应将凡士林涂在旋塞的a端和旋塞套内的c端
B. 滴定前,锥形瓶和滴定管均须用标准溶液润洗
C. 将标准溶液装入滴定管时,应借助烧杯或漏斗等玻璃仪器转移
D. 滴定时,通常用左手控制旋塞滴加溶液,右手摇动锥形瓶,使溶液向同一方向旋转
E. 滴定到终点时俯视读取数据,测得的x值偏大
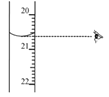
③图中滴定终点时显示的读数为_______ mL。
【答案】A、D、E、F ecbdaf AD 20.60
【解析】
(1)配制一定物质的量浓度的溶液,要经过计算、称量、溶解、移液、洗涤、定容、摇匀等步骤,根据步骤选择仪器;
(2)①滴定时,应先润洗滴定管,调整滴定管液面后再进行滴定;
③滴定管最小刻度为0.1mL,可读到0.01mL。
(1)配制一定物质的量浓度的溶液,要经过计算、称量、溶解、移液、洗涤、定容、摇匀等步骤,称量时需要电子天平,溶解时需要玻璃棒,转移时需要100mL容量瓶,定容时需要胶头滴管,因此答案为A、D、E、F;
(1)①滴定时,应先润洗滴定管,调整滴定管液面后再进行滴定,操作顺序为ecbdaf;
②A、图1中,应将凡士林涂在旋塞的a端和旋塞套内的c端,起润滑和密封作用,A正确;
B、滴定前,滴定管用标准溶液润洗,锥形瓶不能润洗,B错误;
C、将标准溶液装入滴定管时,可用烧杯倾倒,也可用移液管等玻璃仪器转移,不需要漏斗,C错误;
D、滴定时,通常用左手控制旋塞滴加溶液,右手摇动锥形瓶,使溶液向同一方向旋转,操作合理,D正确;
E、滴定到终点时俯视读取数据,导致体积偏小,则测定结果偏小,E错误;
故答案为:AD;
③滴定管最小刻度为0.1mL,可读到0.01mL,由图可知读数为20.60mL。


科目:高中化学 来源: 题型:
【题目】关于下列各装置图的叙述中,不正确的是 ( )
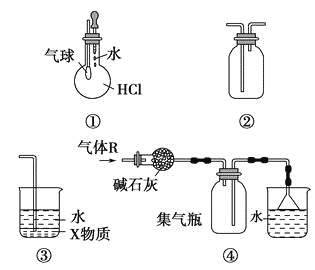
A.装置①可验证HCl气体在水中的溶解性
B.装置②可用于收集H2、NH3、Cl2、HCl、NO2、NO等
C.装置③中X为四氯化碳,可用于吸收氨气或氯化氢
D.装置④可用于干燥、收集氨气,并吸收多余的氨气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】国际计量大会第26届会议修订了阿伏加德罗常数(NA=6.02214076×1023mol-1),于2019年5月2日正式生效。设NA是阿伏加德罗常数的值,下列说法正确的是
A.40g正丁烷和18 g异丁烷的混合物中共价键数目为13NA
B.常温常压下,124 g P4中所含P—P键数目为4NA
C.电解精炼铜时,阳极质量减小3.2g时,转移的电子数为0.1NA
D.0.1mol FeCl3完全水解转化为氢氧化铁胶体,生成胶粒数目为0.1NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.pH=3的盐酸与pH=11的氨水混合,若溶液显中性,则V(盐酸)>V(氨水)
B.室温时某溶液的pH<7,则该物质一定是酸或强酸弱碱盐
C.Na2CO3溶液呈碱性的原因:CO32-+2H2OH2CO3+2OH-
D.0.1 molLˉ1CH3COOH溶液加水稀释,CH3COO- 数目增多,c(OH-)减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2019年是门捷列夫提出元素周期表150周年。已知在元素周期表中,元素Q、R、W、Y与元素X相邻。Y的最高化合价氧化物的水化物是强酸。W与Q可以形成一种高温结构陶瓷材料,W的氯化物分子呈正四面体结构。回答下列问题:
(1)元素X在元素周期表中的位置_________
(2)W的氧化物的晶体类型是____________
(3)R和Y形成的二元化合物中,R呈现最高化合价的化合物的化学式是________
(4)这5个元素的氢化物分子中:
①立体结构类型相同的氢化物的沸点从高到低排列次序是(填化学式)_______
②电子总数相同的氢化物的化学式和立体结构分别是_________
(5)W和Q所形成的结构陶瓷材料的一种合成方法如下:W的氯化物与Q的氢化物加热反应,生成化合物W(QH2)4和HCl气体;W(QH2)4在高温下分解生成Q的氢化物和该陶瓷材料。上述相关反应的化学方程式(各物质用化学式表示)是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产生活息息相关。下列说法不正确的是
A.城市空气质量报告中,PM2.5、PM10指的是悬浮颗粒物,会影响人体健康
B.“静电除尘”、“燃煤固硫”、“汽车尾气催化净化”能提高空气质量
C.食品包装袋中常放入小袋的生石灰,目的是防止食品氧化变质
D.氧化亚铁可以用作色素,如应用于瓷器制作中使釉呈绿色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下可利用甲烷消除氮氧化物的污染,例如:CH4+2NO2N2+CO2+2H2O。在2L密闭容器中,控制在不同温度下,分别加入0.50molCH4和0.90molNO2,测得n(CH4)随时间变化的有关实验数据如下表所示。
组别 | 温度 | n/mol | 时间/min | ||||
0 | 10 | 20 | 40 | 50 | |||
① | T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
② | T2 | n(CH4) | 0.50 | 0.30 | 0.18 | x | 0.15 |
下列说法不正确的是
A.组别①中,0~20min内,NO2的降解速率为0.025mol·L-1·min-1
B.该反应的△H<0
C.40min时,x的数值应为0.15
D.0~20min内NO2的降解百分数①<②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】马尾藻和海带中都含丰富的碘,可从中提取碘单质,实验室选取常见的海带设计并进行了以下实验:

(1)操作①的名称为___________。
A.萃取 B.分液 C.蒸发结晶 D.过滤
(2)步骤③中所用的分液漏斗使用前须进行检漏,试简述其操作______。
(3)步骤②加入H2O2和H2SO4溶液,反应的离子方程式为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纪录片《我在故宫修文物》表现了文物修复者穿越古今与百年之前的人进行对话的职业体验,让我们领略到历史与文化的传承。下列文物修复和保护的过程中涉及化学变化的是( )
A | B | C | D |
|
|
|
|
银器用除锈剂除锈 | 变形的金属香炉复原 | 古画水洗除尘 | 木器表面擦拭烫蜡 |
A.AB.BC.CD.D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com