
科目:高中化学 来源: 题型:
下列说法正确的是
A.强电解质的水溶液中不存在溶质分子,弱电解质的水溶液中存在溶质分子和离子
B.强电解质的水溶液导电性强于弱电解质的水溶液
C.强电解质都是离子化合物,弱电解质都是共价化合物
D.强电解质易溶于水,弱电解质难溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)催化剂能改变反应的焓变 ( )
(2012·江苏,4B)
(2)催化剂能降低反应的活化能 ( )
(2012·江苏,4C)
(3)利用太阳能在催化剂参与下分解水制氢是把光能转化为化学能的绿色化学方法( )
(2012·浙江理综,7A)
(4)化学反应有新物质生成,并遵循质量守恒定律和能量守恒定律 ( )
(2011·浙江理综,7A)
(5)实验测得环己烷(l)、环己烯(l)和苯(l)的标准燃烧热分别为-3 916 kJ·mol-1、
-3 747 kJ·mol-1和-3 265 kJ·mol-1,可以证明在苯分子中不存在独立的碳碳双键( )
(2011·浙江理综,12C)
(6)已知:Fe2O3(s)+3C(石墨)===2Fe(s)+3CO(g)
ΔH=489.0 kJ·mol-1
CO(g)+ O2(g)===CO2(g)
O2(g)===CO2(g)
ΔH=-283.0 kJ·mol-1
C(石墨)+O2(g)===CO2(g)
ΔH=-393.5 kJ·mol-1
则4Fe(s)+3O2(g)===2Fe2O3(s)
ΔH=-1 641.0 kJ·mol-1 ( )
(2011·浙江理综,12D)
(7)开发核能、太阳能等新能源,推广甲醇汽油,使用无磷洗涤剂都可直接降低碳排放
( )
(2010·浙江理综,7B)
(8)500 ℃、300 MPa下,将0.5 mol N2和1.5 mol H2置于密闭容器中充分反应生成NH3(g),放热19.3 kJ,其热化学方程式为N2(g)+3H2(g)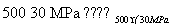 2NH3(g) ΔH=
2NH3(g) ΔH=
-38.6kJ·mol-1 ( )
(2010·浙江理综,12B)
(9)使用太阳能热水器、沼气的利用、玉米制乙醇都涉及到生物质能的利用 ( )
(2009·浙江理综,7C)
(10)石油、煤、天然气、可燃冰、植物油都属于化石燃料 ( )
(2009·浙江理综,7D)
查看答案和解析>>
科目:高中化学 来源: 题型:
断开1 mol AB(g)分子中的化学键使其分别生成气态A原子和气态B原子所吸收的能量称为A—B键的键能。下表列出了一些化学键的键能E:
| 化学键 | H—H | Cl—Cl | O===O | C—Cl | C—H | O—H | H—Cl |
| E/kJ·mol-1 | 436 | 247 | x | 330 | 413 | 463 | 431 |
请回答下列问题:
(1)如图表示某反应的能量变化关系,则此反应为________(填“吸热”或“放热”)反应,其中ΔH=______________(用含有a、b的关系式表示)。
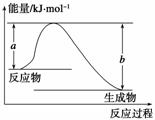
(2)若图示中表示反应H2(g)+ O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1,则b=________kJ·mol-1,x=__________。
O2(g)===H2O(g) ΔH=-241.8 kJ·mol-1,则b=________kJ·mol-1,x=__________。
(3)历史上曾用“地康法”制氯气,这一方法是用CuCl2作催化剂,在450 ℃利用空气中的氧 气跟氯化氢反应制氯气。反应的化学方程式为___________________________。
气跟氯化氢反应制氯气。反应的化学方程式为___________________________。
若忽略温度和压强对反应热的影响,根据上题中的有关数据,计算当反应中有1 mol电 子转移时,反应的能量变化为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
哈伯因发明了由氮气合成氨气的方法而获得1918年诺贝尔化学奖。现向一密闭容器中充入1 mol N2和3 mol H2,在一定条件下使该反应发生。下列有关说法正确的是( )
A.达到化学平衡时,N2将完全转化为NH3
B.达到化学平衡时,N2、H2和NH3的物质的量浓度一定相等
C.达到化学平衡时,N2、H2和NH3的物质的量浓度不再变化
D.达到化学平衡时,正反应和逆反应的速率都为零
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定条件下,对于密闭容器中进行的可逆反应A(g)+3B(g) 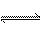
|
A.生成C的速率与C分解的速率相等
B.A、B、C的浓度相等
C.单位时间生成 n mol A,同时生成 3n mol B
D.A、B、C的分子数之比为 1∶3∶2
查看答案和解析>>
科目:高中化学 来源: 题型:
卤代烃A(C2H5X)是一种无色液体,为探究A的性质,设计如下实验方案。
方案一:往A中加入硝酸银溶液,充分振荡,静置。
方案二:往A中加过量NaOH水溶液,充分振荡,静置,待液体分层后,取“水层”溶液少许,滴加硝酸银溶液。
方案三:往A中加入过量NaOH乙醇溶液,共热,充分反应后,取溶液少许,依次加入试剂B、硝酸银溶液,得浅黄色沉淀。
根据以上信息回答问题。
(1)C2H5X中的X是 。 (写化学式)
(2)有人认为方案二达不到检验X-的实验目的,理由是 。
(3)方案三中,试剂B是 。写出方案三中可能发生反应的化学方程式
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子在溶液中能大量共存的一组是
A.Fe3+、H+、ClO-、SO32- B.K+、Al3+、Cl-、CO32-
C.Na+、Ca2+、HCO3-、OH- D.Fe2+、NH4+、NO3-、SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com