
现有常温下的五种溶液(如下表)。

下列有关叙述中正确的是
A.五种溶液中,水电离出的c(OH-)最小的是⑤
B.将①、④两种溶液等体积混合,所得溶液中:c(Cl-)>c(NH4+)>c(OH-)> c(OH-)。
C.分别将①、②、③、④加水稀释100倍,稀释后四种溶液的pH:①>②>③>④
D.在⑤中加入适量的④至溶液呈中性,所得溶液中:c(Na+)>c(CH3COO-)> c(Cl-)>c(OH-)= c(H+)。
D
【解析】
试题分析:A.五种溶液中,①、②、③、④都是对水的电离起抑制作用,而且抑制的程度相同,但是⑤是强碱弱酸盐,对水的电离起促进作用,所以水电离出的c(OH-)最大的是⑤。错误。B.氨水是弱碱,盐酸是强酸。若将①、④两种溶液等体积混合,由于碱过量,所以所得溶液是NH4Cl与NH3·H2O的混合溶液。由于NH3·H2O的电离作用大于NH4Cl的水解作用。所以c(NH4+)>c(Cl-).电离使溶液显碱性,所以c(OH-)>c(H+).盐的电离大于弱电解质的电离作用,因此c(Cl-)>c(OH-)。所以溶液中的两种浓度关系为c(NH4+)>c(Cl-)> c(OH-)>c(H-)。错误。C.①、③是弱电解质,加水稀释时pH变化较小,而②、④是强电解质,加水稀释时pH变化较大。若将这四种溶液加水稀释100倍,稀释后四种溶液的pH:①>②>④>③。错误。D.在⑤中加入适量的④至溶液呈中性,所得溶液是NaCl、CH3COONa、CH3COOH的混合溶液。由于加入的HCl量较小,所以离子浓度关系是c(Na+)>c(CH3COO-)> c(Cl-)>c(OH-)= c(H+)。正确。
考点:考查电离程度相同的强酸、弱酸、强碱、弱碱的稀释的pH变化、溶液混合时的酸碱性及离子浓度变化关系的知识。


 每课必练系列答案
每课必练系列答案科目:高中化学 来源:2013-2014学年上海市徐汇、松江、金山三区高三二模化学试卷(解析版) 题型:选择题
如图是一种有机物的比例模型,该模型代表的有机物可能是
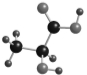
A.饱和一元醇 B.羟基酸 C.羧酸 D.饱和一元醛
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市红桥区高三第二次模拟考试理综化学试卷(解析版) 题型:选择题
室温下,对pH相同、体积相同的醋酸和盐酸两种溶液分别采取下列措施,其中叙述正确的是
A.温度升高20℃后,两溶液pH均不变
B.加适量的醋酸钠晶体后,两溶液的pH均增大
C.加水稀释2倍后,两溶液的pH同等程度减小
D.加足量的锌充分反应后,两溶液中产生的氢气一样多
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市河北区高三总复习质量检测一理综化学试卷(解析版) 题型:简答题
(15分)原子序数由小到大排列的四种短周期元素X、Y、Z、W,四种元素的原子序数之和为32,在周期表中X是原子半径最小的元素,Y、Z左右相邻,Z、W位于同主族。
(1)X元素符号是 ;
(2)Z、W形成的气态氢化物的稳定性_______>_______(写化学式)。
(3)由X、Y、Z、W四种元素中的三种组成的一种强酸,该强酸的稀溶液能与铜反应,离子方程式为___________。
(4)由X、Y、Z、W四种元素组成的一种离子化合物A,已知①1mol A能与足量NaOH浓溶液反应生成标准状况下44.8L气体。②A能与盐酸反应产生气体,该气体能与氯水反应,写出该气体与氯水反应的离子方程式_____________________。
(5)由X、Y、Z、W和Fe五种元素组成的相对分子质量为392的化合物B,lmolB中含有6mol结晶水。对化合物B进行如下实验:
A.取B的溶液加入过量浓NaOH溶液并加热,产生白色沉淀和无色刺激性气味气体;过一段时间白色沉淀变为灰绿色,最终变为红褐色。
B.另取B的溶液,加入过量BaCl2溶液产生白色沉淀,加盐酸沉淀不溶解。
①由实验a、b推知B溶液中含有的离子为__________________;
②B的化学式为_________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市河北区高三年级总复习质量检测三理综化学试卷(解析版) 题型:填空题
(15分)“低碳循环”已引起各国家的高度重视,而如何降低大气中CO2的含量和有效地开发利用CO2正成为化学家研究的主要课题。
(l)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:
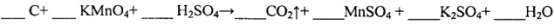
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应 ,得到如下两组数据:
,得到如下两组数据:
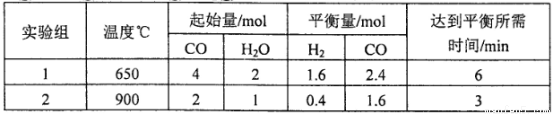
①实验2条件下平衡常数K= __________。
②实验3,若900℃时,在此容器中加入CO、H2O、CO2、H2均为1mol,则此时
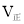 ____________
____________ (填“<”,“>”,“=”)。
(填“<”,“>”,“=”)。
③由两组实验结果,可判断该反应的正反应△H_____________0(填“<”,‘‘>”,“=”)。
(3)己知在常温常压下:
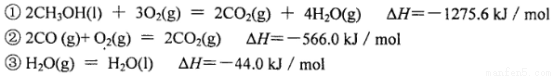
写出甲醇不完全燃烧生成一氧化碳和液态水的热化学方程式:________________________

①已知该反应的△H>0,简述该设想能否实现的依据:________。
②目前,在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为__________。
(5)CO2在自然界循环时可与CaCO3反应,CaCO3是一种难溶物质,其Ksp=2.8× 10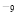 。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为1×10
。CaCl2溶液与Na2CO3溶液混合可形成CaCO3沉淀,现将等体积的CaCl2溶液与Na2CO3溶液混合,若Na2CO3溶液的浓度为1×10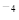 mol/L,则生成沉淀所需CaCl2溶液的最小浓度为__________mol/L。
mol/L,则生成沉淀所需CaCl2溶液的最小浓度为__________mol/L。
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市河东区高三二模考试理综化学试卷(解析版) 题型:填空题
(14分)如下图装置所示,是用氢氧燃料电池B进行的某电解实验:
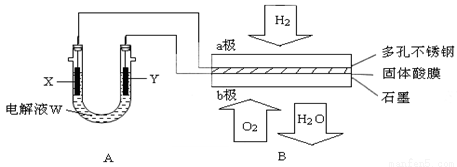
(1)若电池B使用了亚氨基锂(Li2NH)固体作为储氢材料,其储氢原理是:Li2NH+H2=LiNH2+LiH,则下列说法中正确的是________。
A. Li2NH中N的化合价是-1价 B.该反应中H2既是氧化剂又是还原剂
C.Li+ 和H+的离子半径相等 D.此法储氢和钢瓶储氢的原理相同
(2)在电池B工作时:
①若用固体Ca(HSO4)2为电解质传递H+,则电子由________极流出,H+向________极移动。(填“a”或“b”)
②b极上的电极反应式为:________________________________
③外电路中,每转移0.1 mol电子,在a极消耗________上的H2(标准状况下)。
(3)若A中X、Y都是惰性电极,电解液W是滴有酚酞的饱和NaCI溶液,则B工作时:
①电解池中X极上的电极反应式是 ________________________________。
在X极这边观察到的现象是 _____________________________________。
②检验Y电极上反应产物的方法是 _________________________________。
③若A中其它均不改变,只将电极Y换成铁棒,可实现的实验目的是_____________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市河东区高三二模考试理综化学试卷(解析版) 题型:选择题
下列关于甲、乙、丙、丁四个图像的说法中,正确的是
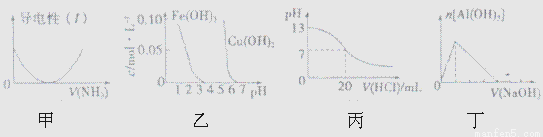
A.图甲表示向乙酸溶液中通入氨气,此过程中溶液导电性的变化
B.由图乙可知,若除去CuSO4溶液中的Fe3+可采用向溶液中加入适量CuO至pH在4左右
C.图丙表示25℃时,用0.1 mol/L盐酸滴定20mL 0.1 mol/L氨水,溶液的pH随加入盐酸体积的变化
D.图丁表示向Al2(SO4)3溶液中滴入NaOH溶液,生成Al(OH)3沉淀的量随NaOH溶液体积的变化
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市高三第五次月考理综化学试卷(解析版) 题型:选择题
控制适合的条件,将反应2Fe3++2I- 2Fe2++I2设计成下图所示的原电池。下列判断不正确的是
2Fe2++I2设计成下图所示的原电池。下列判断不正确的是
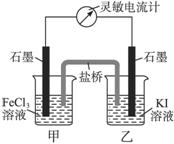
 A. 为证明反应的发生,可取甲中溶液加入酸性高锰酸钾溶液
A. 为证明反应的发生,可取甲中溶液加入酸性高锰酸钾溶液
B. 反应开始时,甲中石墨电极上Fe3+被还原,乙中石墨电极上发生氧化反应
C. 电流计读数为零时,在甲中加入FeCl2固体后,甲中石墨电极为负极
D. 此反应正反应方向若为放热反应,电流计读数为零时,降低温度后,乙中石墨电极为负极
查看答案和解析>>
科目:高中化学 来源:2013-2014天津市下学期期中考试高二化学试卷(解析版) 题型:选择题
下列叙述正确的是________________。
A.不慎把苯酚溶液沾到了皮肤上,应立即用酒精洗涤
B.甲、乙两种有机物具有相同的相对分子质量和不同结构,则甲和乙一定是同分异构体。
C.将浓溴水滴入到苯酚溶液中立即产生2,4,6-三溴苯酚的白色沉淀。
D.将CH3CHO(易溶于水,沸点为20.8℃的液体)和CH3COOH分离的最好的方法是直接蒸馏
E.水的沸点是100℃,酒精的沸点是78.5℃,所以可用直接加热蒸馏法使含水酒精变为无水酒精
F.实验室使用体积比为1:3的浓硫酸与乙醇的混合溶液制乙烯时,为防加热时反应混合液出现暴沸现象,除了要加沸石外,还应注意缓慢加热让温度慢慢升至170℃。
G.除去混在苯中的少量苯酚,加入过量溴水,过滤。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com