
【题目】摩尔浓度相同的三种盐NaX、NaY和NaZ的溶液,其中pH值依次为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是( )
A.HX、HZ、HY
B.HZ、HY、HX
C.HX、HY、HZ
D.HY、HZ、HX
 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案 欣语文化快乐暑假沈阳出版社系列答案
欣语文化快乐暑假沈阳出版社系列答案科目:高中化学 来源: 题型:
【题目】图中每条线表示两端的物质可以发生化学反应,甲、乙、丙、丁分别为Mg、BaCl2、Na2CO3、HCl中的一种,下列说法正确的是

A. 甲是Na2CO3
B. 乙是Mg
C. 反应①②是非氧化还原反应
D. 丙与丁发生反应时,丁是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将30mL 0.5mol/LNaOH溶液加水稀释到500mL,稀释后溶液中NaOH的物质的量浓度为( )
A.0.3 mol/LB.0.03 mol/LC.0.05 mol/LD.0.04 mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如表为长式周期表的一部分,其中的编号代表对应的元素. 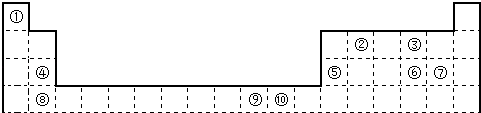
请回答下列问题:
(1)科学家发现,②、④、⑨三种元素的原子形成的晶体具有超导性,其晶胞的结构特点如图所示(图中②、④、⑨分别位于晶胞的体心、顶点、面心),则该化合物的化学式为(用对应的元素符号表示).
(2)某元素的价电子排布式为nsnnpn+1 , 该元素与元素①形成的18电子的X分子的结构式为;该元素还可与元素①形成10电子的气体分子Y,将过量的Y气体通入盛有含⑩元素的硫酸盐溶液中,反应过程中的实验现象为 .
(3)比较③,⑤,⑥,⑦,⑧五种元素的电负性大小,由大到小排列的顺序为(用 元素符号表示).
(4)⑩元素单质晶体采取堆积方式 , 空间利用率为 . 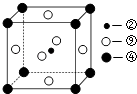
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D是原子序数依次增大的前四周期元素,A是周期表中原子半径最小的元素,它们组成的单质或化合物有如图转化关系,其中甲、丙和戊是单质,乙、丁和己是氧化物,其中丁是两性氧化物,戊是紫红色金属。请回答下列问题:
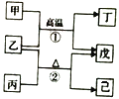
(1)D元素的元素符号为______________,C元素在周期表中的位置为_____________。
(2)用电子式表示己的形成过程_____________。
(3)反应①在工业生产中通常称作_____________反应。
(4)甲、戊与浓硝酸可形成原电池,其中________________(填化学式)作负极,正极电极反应式为__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组中的离子,能在溶液中大量共存的是( )
A.K+、H+、SO42-、OH-B.Na+、Ca2+、CO32-、NO3-
C.Na+、H+、Cl-、CO32-D.Na+、Cu2+、Cl-、SO42-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】胶体与其他分散系的本质区别在于( )
A. 胶体的分散系能通过滤纸空隙,而浊液的分散质不能
B. 分散质粒子直径大小不同
C. 产生丁达尔现象
D. 胶体在一定条件下能稳定存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将mg Al2O3和Fe2O3的混合物溶于100mL盐酸中,然后逐滴加入1mol/LNaOH溶液,其结果如图所示:

(1)最初加入V1mLNaOH溶液的作用是____________;
(2)盐酸的物质的量浓度是___________________;
(3)若mg混合物中Al2O3和Fe2O3按不同比例进行上述实验(其他条件不变),则V2的值会不会改变__________(填“会”或 “不会”),(V2—V1)的取值范围是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com