


科目:高中化学 来源: 题型:
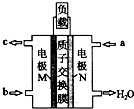 甲醇燃料电池体积小巧、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用.某型甲醇 燃料电池的总反应式2CH40+302=2C02↑+4H20,如图是该燃料电池的示意图.下列说法错误的是( )
甲醇燃料电池体积小巧、洁净环保、理论能量比高,已在便携式通讯设备、汽车等领域应用.某型甲醇 燃料电池的总反应式2CH40+302=2C02↑+4H20,如图是该燃料电池的示意图.下列说法错误的是( )| A、燃料电池将化学能转化为电能 |
| B、a是甲醇,b是氧气 |
| C、质子从M电极区穿过交换膜移向N电极区 |
| D、负极反应:CH40-6e-+H20=C02↑+6H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶度积大的化合物溶解度肯定大 |
| B、向含有AgCl固体的溶液中加入适量的水使溶解又达到平衡时,AgCl的溶度积不变,其溶解度也不变 |
| C、将难溶电解质放入水中,溶解达到平衡时,电解质离子的浓度的乘积就是该物质的溶度积 |
| D、AgCl水溶液的导电性很弱,所以AgCl为弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向水中加入少量固体硫酸氢钠,c(H+)增大,Kw不变 |
| B、向水中加入稀氨水,平衡逆向移动,c(OH-)降低 |
| C、向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| D、将水加热,Kw增大,pH不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔是用于计量微观粒子集体的物理量 |
| B、CO2的摩尔质量为44g |
| C、0.5mol水中约含6.02×1023个H |
| D、标准状况下1 mol任何物质体积均为22.4L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com