
| A. | CaO | B. | CO | C. | SiO2 | D. | H2O |
分析 氧化物是指由两种元素组成的化合物中,其中一种元素是氧元素.与酸溶液反应生成盐和水的化合物为碱性氧化物,与碱溶液反应生成盐和水的化合物为酸性氧化物,两者都能反应的为两性氧化物,两者都不能的为不成盐氧化物,CO2、P2O5、SO2都属于非金属氧化物,能和碱反应生成盐和水,属于酸性氧化物.
解答 解:CO2、P2O5、SO2都属于非金属氧化物,且属于酸性氧化物.
A.CaO属于碱性氧化物,不属于酸性氧化物,故A错误;
B.一氧化碳属于不成盐氧化物,不属于酸性氧化物,故B错误;
C.二氧化硅是非金属氧化物,且属于酸性氧化物,如与氢氧化钠反应生成硅酸钠和水,故C正确;
D.水属于不成盐氧化物,不属于酸性氧化物,故D错误.
故选C.
点评 本题考查了物质的分类中的氧化物,注意掌握不同氧化物的基本概念,并能够区分应用,本考点的基础性比较强,主要出现在选择题和填空题中,题目较简单.


科目:高中化学 来源: 题型:选择题
| A. | ①③④② | B. | ①③②④ | C. | ③④②① | D. | ③①②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
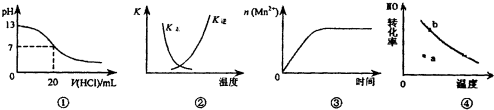
| A. | 图①表示25℃时,用0.1 mol•L-1盐酸滴定20 mL 0,1 mol•L-1 NaOH溶液,溶液的pH随加入酸体积的变化 | |
| B. | 图②中曲线表示反应2SO2(g)+O2(g)?2SO3(g):△H<0正、逆反应的平衡常数K随温度的变化 | |
| C. | 图③表示10 mL 0.01 mol•L-1 KMnO4酸性溶液与过量的0.1 mol•L-1 H2C2O4溶液混合时,n(Mn2+)随时间的变化 | |
| D. | 图④曲线表示2NO+O2?2NO2中NO的最大转化率与温度的关系,a点表示未达到平衡状态,且v(正)<v(逆) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  | B. | 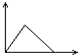 | C. | 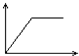 | D. |  |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 镁离子的电子式Mg2+ | B. | Cl的结构示意图 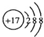 | ||
| C. | 氯离子的电子式Cl- | D. | 质量数为37的氯原子${\;}_{37}^{17}$Cl |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 品红溶液:红色褪去,加热该褪色溶液,仍无色:氯气具有漂白性 | |
| B. | 紫色石蕊溶液:先变红,后褪色;氯气与水反应生成盐酸和次氯酸 | |
| C. | 含酚酞的氢氧化钠溶液:红色褪去;氯气只作氧化剂 | |
| D. | 硫化钠溶液:溶液变浑浊;氯气只作还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
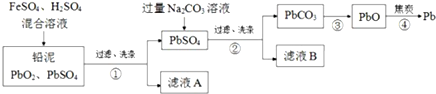
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5 min内D的平均反应速率为0.02 mol•L-1•min-1 | |
| B. | 5 min内A的平均反应速率为0.03 mol•L-1•min-1 | |
| C. | 达平衡后,向容器内再加入少量的A,平衡将向正右移动 | |
| D. | 平衡状态时,生成1molD时同时生成1molA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com