
 ¶ĢÖÜĘŚŌŖĖŲ×é³ÉµÄµ„ÖŹX2£¬Y£®³£ĪĀĻĀ£¬X2ŹĒŅ»ÖÖ»ĘĀĢÉ«ĘųĢ壬YĪŖµ»ĘÉ«¹ĢĢ壬ZŹĒŅ»ÖÖ³£¼ūµÄ¼ī£¬ŃęÉ«·“Ó¦³ŹĒ³×ĻÉ«£ØĶø¹żīܲ£Į§£©ĒŅ0.1mol•L-1 ZµÄĖ®ČÜŅŗpH=13£®X2”¢Y ŗĶZÖ®¼äÓŠČēĶ¼×Ŗ»Æ¹ŲĻµ£ØĘäĖūĪŽ¹ŲĪļÖŹŅŃĀŌČ„£©
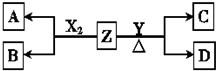
¶ĢÖÜĘŚŌŖĖŲ×é³ÉµÄµ„ÖŹX2£¬Y£®³£ĪĀĻĀ£¬X2ŹĒŅ»ÖÖ»ĘĀĢÉ«ĘųĢ壬YĪŖµ»ĘÉ«¹ĢĢ壬ZŹĒŅ»ÖÖ³£¼ūµÄ¼ī£¬ŃęÉ«·“Ó¦³ŹĒ³×ĻÉ«£ØĶø¹żīܲ£Į§£©ĒŅ0.1mol•L-1 ZµÄĖ®ČÜŅŗpH=13£®X2”¢Y ŗĶZÖ®¼äÓŠČēĶ¼×Ŗ»Æ¹ŲĻµ£ØĘäĖūĪŽ¹ŲĪļÖŹŅŃĀŌČ„£©·ÖĪö ¶ĢÖÜĘŚŌŖĖŲ×é³ÉµÄµ„ÖŹX2ŹĒŅ»ÖÖ»ĘĀĢÉ«ĘųĢ壬ӦĪŖCl2£¬YĪŖĒ³»ĘÉ«¹ĢĢåµ„ÖŹ£¬Ó¦ĪŖS£¬ZŹĒŅ»ÖÖ»ÆŗĻĪļ£¬ŃęÉ«·“Ó¦³ŹĒ³×ĻÉ«£ØĶø¹żīܲ£Į§£©£¬Ó¦ŗ¬ÓŠKŌŖĖŲ£¬ĒŅ³£ĪĀĻĀ£¬0.1mol•L-1ZµÄĖ®ČÜŅŗpH=13£¬ĖµĆ÷ZĪŖŅ»ŌŖĒæ¼ī£¬ŌņZĪŖKOH£¬ÓėĀČĘų·“Ó¦µÄ·½³ĢŹ½ĪŖCl2+2KOH=KCl+KClO+H2O£¬¼ÓČČĢõ¼žĻĀ£¬ĮņÓėKOH·“Ӧɜ³ÉK2S”¢K2SO3£¬ŅŌ“Ė½ā“šøĆĢā£®
½ā“š ½ā£ŗ¶ĢÖÜĘŚŌŖĖŲ×é³ÉµÄµ„ÖŹX2ŹĒŅ»ÖÖ»ĘĀĢÉ«ĘųĢ壬ӦĪŖCl2£¬YĪŖĒ³»ĘÉ«¹ĢĢåµ„ÖŹ£¬Ó¦ĪŖS£¬ZŹĒŅ»ÖÖ»ÆŗĻĪļ£¬ŃęÉ«·“Ó¦³ŹĒ³×ĻÉ«£ØĶø¹żīܲ£Į§£©£¬Ó¦ŗ¬ÓŠKŌŖĖŲ£¬ĒŅ³£ĪĀĻĀ£¬0.1mol•L-1ZµÄĖ®ČÜŅŗpH=13£¬ĖµĆ÷ZĪŖŅ»ŌŖĒæ¼ī£¬ŌņZĪŖKOH£¬ÓėĀČĘų·“Ó¦µÄ·½³ĢŹ½ĪŖCl2+2KOH=KCl+KClO+H2O£¬¼ÓČČĢõ¼žĻĀ£¬ĮņÓėKOH·“Ӧɜ³ÉK2S”¢K2SO3£¬
£Ø1£©±Č½Ļ·Ē½šŹōŠŌ£¬Ó¦øł¾ŻĒā»ÆĪļµÄĪČ¶ØŠŌ”¢µ„ÖŹµÄŃõ»ÆŠŌŅŌ¼°×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļµÄĖįŠŌ£¬Ö»ÓŠBC·ūŗĻ£¬¹Ź“š°øĪŖ£ŗBC£»
£Ø2£©KOHÓėĀČĘų·“Ó¦µÄ·½³ĢŹ½ĪŖCl2+2KOH=KCl+KClO+H2O£¬¹Ź“š°øĪŖ£ŗCl2+2KOH=KCl+KClO+H2O£»
£Ø3£©SŗĶKOH·“Ӧɜ³ÉK2SO3ŗĶK2S£¬ŅŃÖŖCÄÜÓėĮņĖį·“Ӧɜ³ÉÄÜŹ¹Ę·ŗģČÜŅŗĶŹÉ«µÄĘųĢ壬ӦĪŖSO2£¬ŌņCĪŖK2SO3£¬DĪŖK2S£¬DĪŖK2S£¬ĪŖĒæ¼īČõĖįŃĪ£¬·¢ÉśĖ®½ā£ŗSO32-+H2O?HS-+OH-£¬ŌņČÜŅŗ³Ź¼īŠŌ£¬
¹Ź“š°øĪŖ£ŗK2S£» S2-+H2O?HS-+OH-£»
£Ø4£©ÓĆøōĤµē½ā²Ūµē½āAµÄČÜŅŗ£¬Ńō¼«²śÉśCl2£¬ŌņAĪŖKCl£¬µē½āKClČÜŅŗ£¬æÉÉś³ÉĒāĘų”¢ĀČĘųŗĶKOH£¬µē½ā·½³ĢŹ½ĪŖ2Cl-+2H2O$\frac{\underline{\;µē½ā\;}}{\;}$ H2”ü+Cl2”ü+2OH-£¬
¹Ź“š°øĪŖ£ŗ2Cl-+2H2O$\frac{\underline{\;µē½ā\;}}{\;}$ H2”ü+Cl2”ü+2OH-£®
µćĘĄ ±¾Ģāæ¼²éĪŽ»śĪļµÄĶʶĻ£¬ĢāÄæÄѶČÖŠµČ£¬ŠčŅŖѧɜŹģĮ·ÕĘĪÕŌŖĖŲ»ÆŗĻĪļÖŖŹ¶£¬×¢Ņāøł¾ŻĪļÖŹµÄŃÕÉ«”¢ĢŲŹā·“Ó¦µČ½ųŠŠĶʶĻ£¬Ń§Ļ°ÖŠ×¢ÖŲĻą¹Ų»ł“”ÖŖŹ¶µÄ»żĄŪ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
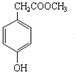 µÄ·Ö×ÓŹ½ŹĒC9H10O3£¬1mol»ÆŗĻĪļIĶźČ«Č¼ÉÕ£¬ĻūŗÄ10molŃõĘų£®
µÄ·Ö×ÓŹ½ŹĒC9H10O3£¬1mol»ÆŗĻĪļIĶźČ«Č¼ÉÕ£¬ĻūŗÄ10molŃõĘų£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ½«NaOH¹ĢĢå·ÅČėČŻĮæĘæÖŠČܽā | |
| B£® | ČܽāNaOHŗ󣬓żČÜŅŗĄäČ“ÖĮŹŅĪĀŗó×ŖŅʵ½ČŻĮæĘæÖŠ | |
| C£® | ¶ØČŻŗ󣬽«ČŻĮæĘæµ¹ÖĆŅ”ŌČ£¬·¢ĻÖŅŗĆę½µµĶ£¬¼ĢŠų¼ÓĖ®ÖĮæĢ¶ČĻß | |
| D£® | ¶ØČŻŹ±ø©ŹÓŅŗĆę£¬ĖłµĆČÜŅŗÅضČĘ«µĶ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 5£ŗ3 | B£® | 5£ŗ4 | C£® | 1£ŗ1 | D£® | 3£ŗ5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ±ł¾§ŹÆ£Ø»ÆѧŹ½ĪŖNa3AlF6£©µÄ¾§Ģå½į¹¹µ„ŌŖČēĶ¼ĖłŹ¾£ØĪ»ÓŚ“óĮ¢·½ĢåµÄ¶ØµćŗĶĆęŠÄ£¬”šĪ»ÓŚ“óĮ¢·½ĢåµÄ12ĢõĄāµÄÖŠµćŗĶ8øöŠ”Į¢·½ĢåµÄĢåŠÄ£©£¬ŅŃÖŖ±ł¾§ŹÆČŪČŚŹ±µēĄė·½³ĢŹ½ĪŖ£ŗNa3AlF6=3Na++AlF${\;}_{6}^{2-}$£¬ÄĒĆ““óĮ¢·½ĢåµÄĢåŠÄ“¦
±ł¾§ŹÆ£Ø»ÆѧŹ½ĪŖNa3AlF6£©µÄ¾§Ģå½į¹¹µ„ŌŖČēĶ¼ĖłŹ¾£ØĪ»ÓŚ“óĮ¢·½ĢåµÄ¶ØµćŗĶĆęŠÄ£¬”šĪ»ÓŚ“óĮ¢·½ĢåµÄ12ĢõĄāµÄÖŠµćŗĶ8øöŠ”Į¢·½ĢåµÄĢåŠÄ£©£¬ŅŃÖŖ±ł¾§ŹÆČŪČŚŹ±µēĄė·½³ĢŹ½ĪŖ£ŗNa3AlF6=3Na++AlF${\;}_{6}^{2-}$£¬ÄĒĆ““óĮ¢·½ĢåµÄĢåŠÄ“¦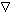 Ėł“ś±ķµÄĪ¢Į£ĪŖ£Ø””””£©
Ėł“ś±ķµÄĪ¢Į£ĪŖ£Ø””””£©| A£® | Na+ | B£® | Al3+ | C£® | F- | D£® | AlF${\;}_{6}^{2-}$ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ŌŚŗ¬ÓŠ“óĮæI-Ąė×ÓµÄČÜŅŗÖŠ£ŗCl?”¢Fe3+”¢Al3+”¢Cu2+ | |
| B£® | ¼ÓČėAlÄܷųöH2µÄČÜŅŗÖŠ£ŗMg2+”¢NH4+”¢Cl-”¢Na+”¢SO42- | |
| C£® | Ź¹pHŹŌÖ½±äÉīĄ¶µÄČÜŅŗÖŠ£ŗCO32-”¢NO3-”¢Na+”¢S2-”¢Al3+”¢SO32- | |
| D£® | ŌŚÓÉĖ®µēĄė³öµÄc£ØH+£©=10-12 mol•L-1µÄČÜŅŗÖŠ£ŗNa+”¢Ba2+”¢Cl?”¢Br? |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | O2 | B£® | CaO | C£® | CH4 | D£® | NaOH |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com