
 A、B、C、D、E五种物质都含同一种元素,C为一种淡黄色的固体化合物.它们按如图所示的关系相互转化,已知A为单质.分别写出有关反应的化学方程式.
A、B、C、D、E五种物质都含同一种元素,C为一种淡黄色的固体化合物.它们按如图所示的关系相互转化,已知A为单质.分别写出有关反应的化学方程式.

科目:高中化学 来源: 题型:
| A、使甲基橙呈红色的溶液中:I-、Cl-、NO3-、Na+ | ||
| B、FeCl3溶液中:K+、Na+、SO42-、AlO2- | ||
C、
| ||
| D、Al2(SO4)3溶液中:K+、Cu2+、Na+、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
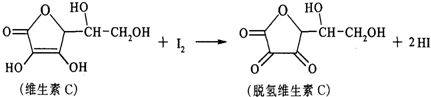
| A、上述反应为取代反应 |
| B、维生素C能抗衰老是因为有氧化性 |
| C、滴定时可用淀粉溶液作指示剂 |
| D、维生素C能发生银镜反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(H+) |
| c(OH-) |
| A、该溶液PH=8 |
| B、0.1mol/L氨水与0.1mol/L HCl溶液混合后所得溶液中:c(NH4+)=c(Cl-) |
| C、若0.1mol/L的氨水与0.05mol/L H2SO4溶液混合后所得溶液PH=7,则V(氨水)>V(H2SO4溶液) |
| D、浓度均为0.1mol/L的NH3?H2O和NH4Cl溶液等体积混合后,若溶液呈碱性,则c(NH4+)>c(NH3?H2O)>c(Cl-)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 化学对人类社会进步和发展的贡献之一是发现和研制了各种材料,例如,金属就是我们生活中不可或缺的重要材料,根据你学过的有关金属的知识,回答下列问题:
化学对人类社会进步和发展的贡献之一是发现和研制了各种材料,例如,金属就是我们生活中不可或缺的重要材料,根据你学过的有关金属的知识,回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、将铜屑加入Fe3+溶液中:2Fe+Cu═2Fe2++Cu2+ |
| B、酸性硫酸亚铁溶液中加入双氧水:Fe2++H2O2+2H+=Fe3++2H2O |
| C、将氯化铝溶液与过量的氨水反应:Al3++4NH3?H2O=AlO2-+4NH4++2H2O |
| D、将铁粉加入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com