
| A. | 向某溶液中加稀盐酸生成无色气体,说明原溶液中有HCO3- | |
| B. | 向某溶液中加BaCl2溶液生成白色沉淀,说明原溶液中有CO32- | |
| C. | 向某溶液中加NaOH溶液微热,产生使湿润的红色石蕊试纸变蓝说明原溶液中有NH4+ | |
| D. | 向某溶液中加稀硫酸生成白色沉淀,说明原溶液中有Ba2+ |
分析 A.无色气体可能为二氧化碳或二氧化硫;
B.白色沉淀可能为AgCl;
C.产生使湿润的红色石蕊试纸变蓝的气体为氨气;
D.白色沉淀可能为硫酸银等.
解答 解:A.无色气体可能为二氧化碳或二氧化硫,则向某溶液中加稀盐酸生成无色气体,说明原溶液中可能有HCO3-或CO32-、HSO3-等,故A错误;
B.白色沉淀可能为AgCl,则向某溶液中加BaCl2溶液生成白色沉淀,说明原溶液中可能有CO32-或Ag+,但二者不能同时存在,故B错误;
C.产生使湿润的红色石蕊试纸变蓝的气体为氨气,则向某溶液中加NaOH溶液微热,产生使湿润的红色石蕊试纸变蓝说明原溶液中有NH4+,故C正确;
D.白色沉淀可能为硫酸银等,则向某溶液中加稀硫酸生成白色沉淀,说明原溶液中有Ba2+或Ag+等,故C错误;
故选C.
点评 本题考查常见离子的检验,为高频考点,把握离子检验的试剂、现象和结论为解答的关键,侧重分析与应用能力的考查,注意离子检验时排除干扰离子,题目难度不大.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在同温同压时,相同体积的任何气体单质所含的分子数目相同 | |
| B. | 2g氢气所含原子数目为NA | |
| C. | 在常温常压下,11.2L氮气所含的原子数目为NA | |
| D. | 17g氨气所含氢原子数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| A组 | B组 | C组 | D组 | |
| 分类标准 | 金属氧化物 | 金属单质 | ||
| 不属于该类别的物质 | Cu | H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | N2为0.2mol/L,H2为0.6mol/L | B. | N2为0.15mol/L | ||
| C. | N2、H2均为0.18mol/L | D. | NH3为0.4mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
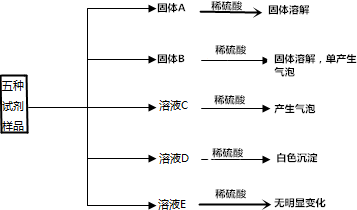 有5瓶白色固体试剂,分别是BaCl2、NaOH、Mg(OH)2、Na2CO3、BaCO3.现分别取少量试剂进行下列实验.请回答下列问题:
有5瓶白色固体试剂,分别是BaCl2、NaOH、Mg(OH)2、Na2CO3、BaCO3.现分别取少量试剂进行下列实验.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1 mol Na2O2与足量CO2反应后转移的电子数为NA | |
| B. | 1 mol Fe被氧化时,失去的电子数一定为2 NA | |
| C. | 常温常压下,11.2 L CH4中含有的氢原子数为2 NA | |
| D. | 0.1 mol/L MgCl2溶液中Cl-离子数为0.2 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3.2mol/L | B. | 1.6mol/L | C. | 0.9mol/L | D. | 无法判断 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com