
 Ņ»¶ØĪĀ¶ČĻĀ2LµÄŗćČŻČŻĘ÷¼×ÖŠ£¬¼ÓČė2moLĢ¼ŗĶ2moLCO2·¢ÉśČēĻĀ·“Ó¦£ŗ
Ņ»¶ØĪĀ¶ČĻĀ2LµÄŗćČŻČŻĘ÷¼×ÖŠ£¬¼ÓČė2moLĢ¼ŗĶ2moLCO2·¢ÉśČēĻĀ·“Ó¦£ŗ·ÖĪö £Ø1£©øł¾Ż·“Ó¦Ē°ŗóĘųĢåµÄĪļÖŹµÄĮæ±ä»Æ·ÖĪö£»øł¾Ż”÷G=”÷H-T”÷S£¼0×Ō·¢·ÖĪöÅŠ¶Ļ£»
£Ø2£©Ņ»¶ØĪĀ¶ČĻĀ2LµÄŗćČŻČŻĘ÷¼×ÖŠ£¬¼ÓČė2moLĢ¼ŗĶ2moLCO2·¢Éś·“Ó¦£¬Ę½ŗāŹ±CO2ĪŖ0.76mol£¬ĮŠČż¶ĪŹ½Ēó³öĘ½ŗāŹ±ø÷ĘųĢåµÄÅØ¶Č£¬ŌŁøł¾ŻĘ½ŗā³£ŹżK=$\frac{c{\;}^{2}£ØCO£©}{c£ØCO{\;}_{2}£©}$¼ĘĖć£»
£Ø3£©øĆ·“Ó¦ÖŠ·½ĻņĪŖĢå»żŌö“óµÄ·½Ļņ£¬ŌŁĶØČė2moLCO2£¬ĢåĻµŃ¹ĒæŌö“ó£¬Ę½ŗāÄęŅĘ£¬ŅĄ“Ė·ÖĪö×Ŗ»ÆĀŹ£»
£Ø4£©øł¾Ż¼ÓČėµÄCO2ŗĶCOµÄÅضČĒó³öQc=$\frac{c{\;}^{2}£ØCO£©}{c£ØCO{\;}_{2}£©}$£¬øł¾ŻQcÓėKµÄ¹ŲĻµÅŠ¶Ļ£»
£Ø5£©ĻņøĆČŻĘ÷¼ÓČė4moLĢ¼ŗĶ4moLCO2£¬“ļµ½Ę½ŗāŹ±CO2ĪļÖŹµÄĮæĪŖ2moL£¬ÓÉÓŚ·“Ó¦ĪļÅضČŌö“ó£¬Ę½ŗāĖłÓĆŹ±¼äĖõ¶Ģ£¬¾Ż“Ė×÷Ķ¼£®
½ā“š ½ā£ŗ£Ø1£©ĘųĢåµÄĪļÖŹµÄĮæŌ½“ó£¬ŌņĢåĻµµÄģŲŌ½“ó£¬ŅŃÖŖC£Øs£©+CO2£Øg£©?2CO£Øg£©Õż·½ĻņĪŖĘųĢåĪļÖŹµÄĮæŌö“óµÄ·½Ļņ£¬ĖłŅŌøĆ·“Ó¦µÄ”÷S£¾0£»ÓÖ”÷G=”÷H-T”÷S£¼0×Ō·¢£¬ŌŁÓÉ”÷H£¾0£¬”÷S£¾0£¬ĖłŅŌŌŚ½ĻøßĪĀ¶ČĻĀÓŠĄūÓŚøĆ·“Ó¦×Ō·¢½ųŠŠ£¬¹Ź“š°øĪŖ£ŗ£¾£»½Ļøߣ»
£Ø2£©ÓÉĶ¼ĻóæÉÖŖĘ½ŗāŹ±CO2ĪŖ0.76mol£»
C£Øs£©+CO2£Øg£©?2CO£Øg£©
³õŹ¼Įæ£Ømol£©£ŗ2 2 0
×Ŗ»ÆĮæ£Ømol£©£ŗ1.24 1.24 2.48
Ę½ŗāĮæ£Ømol£©£ŗ0.76 0.76 2.48
ŌņĘ½ŗāŹ±ø÷ĘųĢåĪļÖŹµÄÅضČĪŖ£ŗc£ØCO2£©=$\frac{0.76mol/L}{2L}$=0.38mol/L£¬c£ØCO£©=$\frac{2.48mol/L}{2L}$=1.24mol/L£»
ĖłŅŌK=$\frac{c{\;}^{2}£ØCO£©}{c£ØCO{\;}_{2}£©}$=$\frac{1.24{\;}^{2}}{0.38}$=4.0£»
¹Ź“š°øĪŖ£ŗ4.0£»
£Ø3£©øĆ·“Ó¦ÖŠ·½ĻņĪŖĢå»żŌö“óµÄ·½Ļņ£¬ŌŁĶØČė2moLCO2£¬ĢåĻµŃ¹ĒæŌö“ó£¬ÓėŌĘ½ŗā±Č½Ļ£¬Ļąµ±ÓŚĘ½ŗāÄęŅĘ£¬ĖłŅŌ¶žŃõ»ÆĢ¼µÄ×Ŗ»ÆĀŹ¼õŠ”£»
¹Ź“š°øĪŖ£ŗ¼õŠ”£»
£Ø4£©ĻąĶ¬ĪĀ¶ČĻĀ£¬2LµÄŗćČŻČŻĘ÷±ūÖŠ¼ÓČė4moLĢ¼”¢4moLCO2ŗĶ4moLCO£¬ŌņæŖŹ¼Ź±c£ØCO2£©=2mol/L£¬c£ØCO£©=2mol/L£¬
Qc=$\frac{c{\;}^{2}£ØCO£©}{c£ØCO{\;}_{2}£©}$=$\frac{2{\;}^{2}}{2}$=2£¼K£¬Ōņ·“Ó¦Ī““ļµ½Ę½ŗā£¬·“Ó¦ÕżĻņ½ųŠŠ£¬ĖłŅŌv£ØÕż£©£¾v£ØÄę£©£»
¹Ź“š°øĪŖ£ŗ£¾£»
£Ø5£©ĻņøĆČŻĘ÷¼ÓČė4moLĢ¼ŗĶ4moLCO2£¬“ļµ½Ę½ŗāŹ±CO2ĪļÖŹµÄĮæĪŖ2moL£¬ÓÉÓŚ·“Ó¦ĪļÅضČŌö“ó£¬Ę½ŗāĖłÓĆŹ±¼äĖõ¶Ģ£¬Ķ¼ĻóĪŖ£ŗ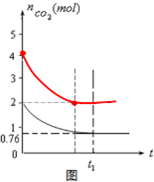 £¬¹Ź“š°øĪŖ£ŗ
£¬¹Ź“š°øĪŖ£ŗ £®
£®
µćĘĄ ±¾Ģāæ¼²éĮĖģŲ±ä”¢Ę½ŗā³£Źż”¢»ÆŃ§Ę½ŗāÓ°ĻģŅņĖŲÓė»ÆŃ§Ę½ŗāĶ¼ĻóµČ£¬×¢Ņāøł¾Ż·“Ó¦µÄĢŲÕ÷·ÖĪöĶā½ēĢõ¼ž¶ŌĘ½ŗāµÄÓ°Ļģ£¬ÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | æÉŅŌĶعż¹żĀĖµÄ·½·Ø½«µķ·Ū½ŗĢåÖŠ»ģÓŠµÄĀČ»ÆÄĘČÜŅŗ³żČ„ | |
| B£® | ·ÖÉ¢ÖŹĮ£×ÓµÄÖ±¾¶£ŗFe£ØOH£©3Šü×ĒŅŗ£¾Fe£ØOH£©3½ŗĢ壾FeCl3ČÜŅŗ | |
| C£® | Ņ»ŹųĘ½ŠŠ¹āĻßÉäČėµ°°×ÖŹČÜŅŗĄļ£¬“Ó²ąĆęæÉŅŌ擵½Ņ»Ģõ¹āĮĮµÄĶØĀ· | |
| D£® | ÖʱøFe£ØOH£©3½ŗĢåµÄ·½·ØŹĒ½«±„ŗĶFeCl3ČÜŅŗµĪ¼Óµ½·ŠĖ®ÖŠÖó·ŠÖĮČÜŅŗ³ŹŗģŗÖÉ« |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
 £®
£® £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ÖŠŗĶČȵďµŃé¹ż³ĢÖŠ£¬»·ŠĪ²£Į§½Į°č°ō²ÄĮĻČōÓĆĶ“śĢę£¬Ōņ²āĮæ³öµÄÖŠŗĶČČŹżÖµĘ«Š” | |
| B£® | ×¼Č·²āĮæÖŠŗĶČȵďµŃé¹ż³ĢÖŠ£¬ÖĮÉŁŠč²ā¶ØĪĀ¶Č4“Ī | |
| C£® | ±ķŹ¾ÖŠŗĶČȵÄČČ»Æѧ·½³ĢŹ½£ŗH+£Øl£©+OH-£Øl£©ØTH2O£Øl£©”÷H=-57.3 kJ/mol | |
| D£® | ŅŃÖŖ2NaOH£Øaq£©+H2SO4£Øaq£©ØTNa2SO4£Øaq£©+2H2O£Øl£©”÷H=-114.6 kJ/mol£¬ŌņøĆ·“Ó¦µÄÖŠŗĶČČĪŖ114.6 kJ/mol |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ŗĶ
ŗĶ Į½ÖÖ½į¹¹Ź½»„ĪŖĶ¬·ÖŅģ¹¹Ģå£Øa”¢bĪŖ²»Ķ¬µÄŌ×Ó»ņŌ×ÓĶÅ£©£¬±»³ĘĪŖĻ©ĢžµÄĖ³·“Ņģ¹¹£¬ŹŌĶʶĻŅ»ĀȱūĻ©µÄĶ¬·ÖŅģ¹¹Ģå£Ø²»ŗ¬»·×“½į¹¹£©¹²ÓŠ£Ø””””£©
Į½ÖÖ½į¹¹Ź½»„ĪŖĶ¬·ÖŅģ¹¹Ģå£Øa”¢bĪŖ²»Ķ¬µÄŌ×Ó»ņŌ×ÓĶÅ£©£¬±»³ĘĪŖĻ©ĢžµÄĖ³·“Ņģ¹¹£¬ŹŌĶʶĻŅ»ĀȱūĻ©µÄĶ¬·ÖŅģ¹¹Ģå£Ø²»ŗ¬»·×“½į¹¹£©¹²ÓŠ£Ø””””£©| A£® | 3ÖÖ | B£® | 4ÖÖ | C£® | 5ÖÖ | D£® | 6ÖÖ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
 ŌŚµē½āÖŹČÜŅŗµÄµ¼µēŠŌ×°ÖĆ£ØČēĶ¼ĖłŹ¾£©ÖŠ£¬ČōĻņijŅ»µē½āÖŹČÜŅŗÖŠÖšµĪ¼ÓČėĮķŅ»ČÜŅŗ£¬ŌņµĘÅŻÓÉĮĮ±ä°µÖĮĻØĆš£¬ŗóÓÖÖš½„±äĮĮµÄŹĒ£Ø””””£©
ŌŚµē½āÖŹČÜŅŗµÄµ¼µēŠŌ×°ÖĆ£ØČēĶ¼ĖłŹ¾£©ÖŠ£¬ČōĻņijŅ»µē½āÖŹČÜŅŗÖŠÖšµĪ¼ÓČėĮķŅ»ČÜŅŗ£¬ŌņµĘÅŻÓÉĮĮ±ä°µÖĮĻØĆš£¬ŗóÓÖÖš½„±äĮĮµÄŹĒ£Ø””””£©| A£® | ŃĪĖįÖŠÖšµĪ¼ÓČėŹ³ŃĪČÜŅŗ | B£® | ĮņĖįÖŠÖšµĪ¼ÓČėNaOHČÜŅŗ | ||
| C£® | ĮņĖįÖŠÖšµĪ¼ÓČėBa£ØOH£©2ČÜŅŗ | D£® | ĮņĖįĶČÜŅŗÖŠÖšµĪ¼ÓČėNaOHČÜŅŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ł¢Ś¢Ū | B£® | ¢Ł¢Ū¢Ż | C£® | ¢Ś¢Ū¢Ż | D£® | ¢Ś¢Ü¢Ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ÓŠŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄA”¢B”¢C”¢D”¢E”¢F”¢G ĘßÖÖŌŖĖŲ£¬A ŹĒ¶ĢÖÜĘŚÖŠ×åŠņŹżµČÓŚÖÜĘŚŹżµÄ·Ē½šŹōŌŖĖŲ£»B ŌŖĖŲµÄŌ×Ó¼Č²»Ņ׏§Č„Ņ²²»Ņ׵Ƶ½µē×Ó£¬Ę仳Ģ¬Ō×ÓÖŠĆæÖÖÄܼ¶µē×ÓŹżĻąĶ¬£»D µÄ×īĶā²ćµē×ÓŹżÓėµē×Ó²ćŹżÖ®±ČĪŖ3£ŗ1£»EŹĒµŲæĒÖŠŗ¬ĮæµŚ¶ž¶ąµÄ·Ē½šŹōŌŖĖŲ£»D”¢FĶ¬×壻 G ŌŖĖŲŌ×ÓŠņŹżĪŖ24£®
ÓŠŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄA”¢B”¢C”¢D”¢E”¢F”¢G ĘßÖÖŌŖĖŲ£¬A ŹĒ¶ĢÖÜĘŚÖŠ×åŠņŹżµČÓŚÖÜĘŚŹżµÄ·Ē½šŹōŌŖĖŲ£»B ŌŖĖŲµÄŌ×Ó¼Č²»Ņ׏§Č„Ņ²²»Ņ׵Ƶ½µē×Ó£¬Ę仳Ģ¬Ō×ÓÖŠĆæÖÖÄܼ¶µē×ÓŹżĻąĶ¬£»D µÄ×īĶā²ćµē×ÓŹżÓėµē×Ó²ćŹżÖ®±ČĪŖ3£ŗ1£»EŹĒµŲæĒÖŠŗ¬ĮæµŚ¶ž¶ąµÄ·Ē½šŹōŌŖĖŲ£»D”¢FĶ¬×壻 G ŌŖĖŲŌ×ÓŠņŹżĪŖ24£®²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com