
【题目】室温下,有pH均为9体积均为10mL的NaOH溶液和CH3COONa溶液,下列说法正确的是( )
A.两种溶液中的c(Na+)相等
B.两溶液中由水电离出的c(OH﹣)之比为 ![]()
C.分别加水稀释到100mL时,两种溶液的pH依然相等
D.分别与同浓度的盐酸反应,恰好反应时消耗的盐酸体积相等
【答案】B
【解析】解:pH相等的NaOH和CH3COONa溶液,c(NaOH)<c(CH3COONa),相同体积、相同pH的这两种溶液,则n(NaOH)<n(CH3COONa),
A.pH相等的NaOH和CH3COONa溶液,c(NaOH)<c(CH3COONa),钠离子不水解,所以钠离子浓度NaOH<CH3COONa,故A错误;
B.酸或碱抑制水电离,含有弱离子的盐促进水电离,NaOH溶液中c(H+)等于水电离出c(OH﹣)=10﹣9 mol/L,CH3COONa溶液 ![]() mol/L=10﹣5 mol/L,两溶液中由水电离出的c(OH﹣)之比=
mol/L=10﹣5 mol/L,两溶液中由水电离出的c(OH﹣)之比= ![]() ,故B正确;
,故B正确;
C.加水稀释促进醋酸钠水解,导致溶液中pH大小为CH3COONa>NaOH,故C错误;
D.分别与同浓度的盐酸反应,恰好反应时消耗的盐酸体积与NaOH、CH3COONa的物质的量成正比,n(NaOH)<n(CH3COONa),所以醋酸钠消耗的稀盐酸体积大,故D错误;
故选B.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列物质的转化在给定条件下能实现的是( ) ①NaAlO2(aq) ![]() AlCl3
AlCl3 ![]() Al
Al
②NH3 ![]() NO
NO ![]() HNO3
HNO3
③NaCl(饱和) ![]() NaHCO3
NaHCO3 ![]() Na2CO3
Na2CO3
④FeS2 ![]() SO3
SO3 ![]() H2SO4 .
H2SO4 .
A.②③
B.①④
C.②④
D.③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“水煤气(CO、H2)﹣空气”燃料电池的工作原理如图所示,其中a、b均
为惰性电极.下列叙述正确的是( )
A.甲处通入的是空气,乙处通入的是水煤气
B.a电极发生还原反应,b电极发生氧化反应
C.用该电池电镀铜,若待镀金属增重6.4g,至少消耗标准状况下的水煤气2.24L
D.a电极的反应式包括:CO+4OH﹣+2e﹣═CO32﹣+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、NH、Cl-、Mg2+、Ba2+、CO![]() 、SO
、SO![]() ,现取三份各100 mL溶液分别进行如下实验:
,现取三份各100 mL溶液分别进行如下实验:
(1)第一份加入AgNO3溶液有沉淀产生
(2)第二份加足量NaOH溶液加热后,收集到气体0.04 mol
(3)第三份加足量BaCl2溶液后,得干燥沉淀6.27 g,经足量盐酸洗涤、干燥后,沉淀质量为2.33 g.根据上述实验,以下推测正确的是
A. K+一定存在 B. 100 mL溶液中含0.01 mol CO![]()
C. Cl-一定存在 D. Ba2+一定不存在,Mg2+可能存在
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】不用其它任何试剂鉴别下列5种物质的溶液:①KOH ②MgSO4 ③Ba(NO3)2 ④CuCl2 ⑤KNO3,被鉴别出来的正确顺序是
A. ⑤④③②① B. ④①②③⑤ C. ②③①④⑤ D. ④①⑤②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验室仅有如下仪器或用品:烧杯、铁架台、铁圈、三脚架、漏斗、分液漏斗、石棉网、酒精灯、玻璃棒、量筒、蒸发皿、圆底烧瓶、火柴。从缺乏仪器或用品的角度看,不能进行的实验项目是( )
A.蒸发
B.萃取
C.液体过滤
D.升华
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在A1C13和MgCl2的混合溶液中,逐滴加入NaOH溶液直至过量,经测定,加入NaOH的体积和所得沉淀的物质的量的关系如图所示(b处NaOH的体积为l L)
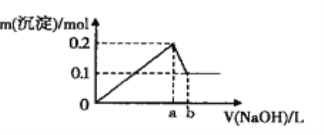
则下列判断正确的是
A. 图中线段oa:ab=3:l B. NaOH溶液物质的量浓度为0.6 mol·L-1
C. 在b点处溶液中的溶质只有NaAlO2 D. 混合溶液中Al3+与Mg2+物质的量比值为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】含铬化合物的废水有毒,特别是Cr(Ⅵ)有致癌作用,对农作物及微生物的毒害很大.目前处理的方法较多,还原沉淀法是较为广泛的处理含铬废水的方法,流程如图: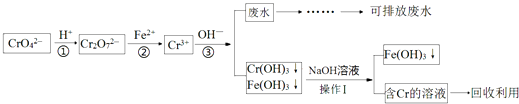
(1)步骤①中存在平衡:2CrO42﹣(黄色)+2H+Cr2O72﹣(橙色)+H2O该反应的平衡常数表达式K=;碱性溶液中Cr(Ⅵ)离子的颜色呈 . (填“黄色”或“橙色”)
(2)上述操作Ⅰ的名称为 , 以下物质可用于代替步骤②中的Fe2+的是
A.KMnO4(H+) B.HNO3 C.Na2SO3
(3)步骤③中出水总铬与溶液的pH关系如图,下列说法不正确的是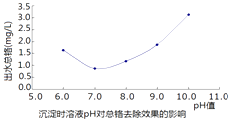
A.为有效除去Cr3+ , 加入的碱越多越好
B.Cr(OH)3可溶于强碱
C.要除去Cr3+ , 调节pH值最好为7左右
(4)已知Ksp[Cr(OH)3]=1.1×10﹣32 , 按《污水综合排放标准》,水质中总铬的浓度应小于3×10﹣5molL﹣1 , 当步骤③调节pH=6时,该处理后的污水是否达到排放标准?(填“是”或“否”).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com