
【题目】苯乙烯(![]() )是生产各种塑料的重要单体,可通过乙苯催化脱氢制得:
)是生产各种塑料的重要单体,可通过乙苯催化脱氢制得:![]()
![]()
![]() +H2(g)
+H2(g)
(1)已知:
化学键 | C-H | C-C | C=C | H-H |
键能/kJ/mol | 412 | 348 | 612 | 436 |
计算上述反应生成1mol氢气的热效应___(填吸放多少kJ)
(2)工业上,通常在乙苯(EB)蒸气中掺混N2(原料气中乙苯和N2的物质的量之比为1︰10,N2不参与反应),控制反应温度600℃,并保持体系总压为0.1Mpa不变的条件下进行反应。在不同反应温度下,乙苯的平衡转化率和某催化剂作用下苯乙烯的选择性(指除了H2以外的产物中苯乙烯的物质的量分数)示意图。
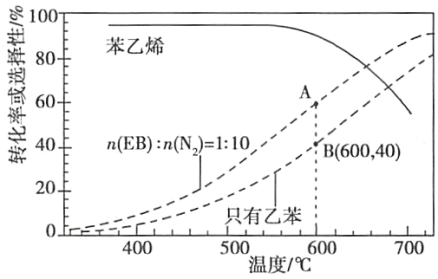
①A、B两点对应的正反应速率较大的是___。
②控制反应温度为600℃的理由是___。
【答案】吸124kJ B 600℃时,乙苯的转化率和苯乙烯的选择性均较高。温度过低,反应速率慢,转化率低;温度过高,选择性下降。高温还可能使催化剂失活,且能耗更高
【解析】
利用反应物的键能总和减去生成物的键能总和的值计算反应的反应热;利用A、B两点压强和温度相同体积不同的特征判断A、B两点的速率大小;根据600℃时反应的转化率和选择性均较高这一特性分析。
(1)反应的热效应可以利用键能大小计算,利用反应物的键能总和减去生成物的键能总和即可得到反应的热效应,当计算结果为正值时为吸热反应,反之则为放热反应;在本反应中由于苯基在反应前后不变,因此苯基的能量在反应前后相同,只需要计算乙基变成乙烯基的能量变化差值即可,即反应的热效应=(348+412×5)kJ/mol-(612+412×3+436)kJ/mol=124kJ/mol,故反应生成1mol氢气的热效应为吸收124kJ的能量;
(2)①根据图像可知,A、B两点的温度和压强都相等,但B点乙苯的浓度大于A点,反应浓度越大,反应速率越快,正反应速率B点大于A点;
②有图可知,600℃时,乙苯的转化率和苯乙烯的选择性均较高,该反应为吸热反应,温度过低,反应速率较慢,乙苯的平衡转化率低,若温度过高,苯乙烯的转化率下降,高温可能使催化剂的活性降低,且耗能大,所以控制温度在600℃。


 小学教材完全解读系列答案
小学教材完全解读系列答案科目:高中化学 来源: 题型:
【题目】甲、乙、丙三种物质均含有同一种中学常见元素X,其转化关系如下,下列说法不正确的是
![]()
A.若A为硝酸,X为金属元素,则甲与丙反应可生成乙
B.若乙为NaHCO3,则丙一定是CO2
C.若A为NaOH溶液,X为短周期的金属元素,则乙一定为白色沉淀
D.若A为金属单质,乙的水溶液遇KSCN溶液变红,则甲可能为非金属单质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由短周期前10号元素组成的物质T和X,存在如图所示的转化关系。X不确定,易分解。下列有关说法正确的是
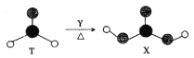
A.为使该转化成功进行,Y可以是酸性KMnO4溶液
B.等物质的量的T、X分子中含有π键的数目均为NA
C.T、X分子中的![]() 原子分别采用sp2杂化和sp3杂化
原子分别采用sp2杂化和sp3杂化
D.T分子中只含有极性键,X分子中既含有极性键又含有非极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X是第四周期元素,最外层只有1个电子,次外层的所有原子轨道均充满电子。元素Y基态原子的3p轨道上有2个未成对电子。元素Z 的原子最外层电子数是其内层的3倍。回答下列问题:
(1)元素X在元素周期表中位于___区,单质X的晶体类型为_____,其中X原子的配位数为_____。
(2)Z的氢化物在乙醇中的溶解度大于Y的氢化物,其原因是__________。
(3)X的氯化物与氨水反应可形成配合物[X(NH3)4]Cl2,1mol该配合物中含有σ键的数目为____________。
(4)X与Y形成的一种化合物的立方晶胞如图所示。
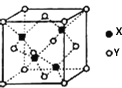
该化合物的化学式为_______,已知此晶体的密度为ρg·cm–3,阿伏伽德罗常数为NA,则此晶胞中X与Y的最近距离是______cm。(写出计算式,不要求计算结果。)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1 L的密闭容器中,充入1 mol CO2和3 mol H2,在500℃时发生反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g) △H<0。CH3OH的浓度随时间变化如图所示,下列说法不正确的是
CH3OH(g)+H2O(g) △H<0。CH3OH的浓度随时间变化如图所示,下列说法不正确的是

A.从反应开始到10min时,H2的平均反应速率v(H2)=0.15 mol/(L·min)
B.从20min到25min达到新的平衡,可能是增大压强
C.其他条件不变,将温度升到700℃,再次达平衡时平衡常数减小
D.从开始到25min,CO2的转化率是70%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在一个2L的密闭容器中,A、B、C三种气体物质的浓度随时间的变化曲线如图所示。根据图中数据,试填写下列空白:
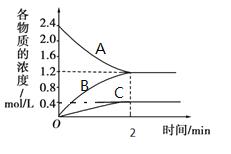
(1)该反应的化学方程式为__。
(2)从开始至2min,B的平均反应速率为__。
(3)下列叙述能说明该反应已达到化学平衡状态的是(填标号)__。
A.A、B、C的物质的量之比为3:1:3
B.相同时间内消耗3molA,同时生成3molC
C.相同时间内消耗3nmolA,同时消耗nmol的B
D.混合气体的总质量不随时间的变化而变化
E.B的体积分数不再发生变化
(4)在某一时刻采取下列措施能使该反应速率减小的是___。
A.加催化剂
B.降低温度
C.体积不变,充入A
D.体积不变,从容器中分离出A
(5)改变影响平衡的一个条件,5分钟后又建立了新平衡,发现C占平衡混合气的体积分数为![]() ,则反应物A的分解率为___。
,则反应物A的分解率为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是生物体内四种有机物的组成与功能关系图,有关叙述不正确的是 ( )
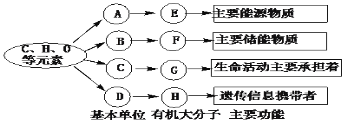
A. 玉米种子细胞中,物质A和E分别代表葡萄糖和纤维素
B. 相同质量的E和F彻底氧化分解,释放能量较多的是F
C. 在人体细胞中物质C约有20种
D. 不同的H在结构上的区别主要是碱基的排列顺序不同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】石棉的化学式可表示为3MgO·2SiO2·2H2O,具有高抗张强度、高挠性耐化学和热浸蚀、电绝缘及具有可纺性的硅酸盐类矿物产品。其中IIA族的元素属于碱土金属。回答下列问题:
(1)与Ca同周期的基态Fe原子的价电子排布式为___________。
(2)BeCl2易升华,液态时以双聚分子存在的BeCl2结构式为___________,其中Be的配位数为___________。
(3)化学式3MgO·2SiO2·2H2O中电负性最大的元素为__________。
SiO2的熔沸点远高于H2O,说明理由:____________________________________________。
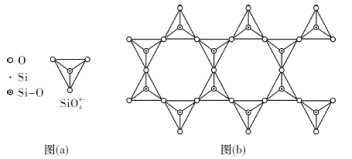
(4)天然硅酸盐组成复杂,阴离子的基本结构单元是SiO44-四面体,如图(a),通过共用顶角氧离子可形成链状、网状等结构,图(b)为一种无限长双链的多硅酸根,其中O与Si的原子数之比为___________,化学式为___________。
(5)经X射线分析鉴定,某一离子晶体属于立方晶系。晶胞顶点位置为Ti4+所占,体心位置为Ba2+所占,所有棱心位置为O2-所占,写出此晶体的化学式:___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求填空:
(1)某烷烃A,其蒸气密度是相同状况下氢气密度的64倍,经测定得知A分子中共含有6个甲基。
①若A不是烯烃与氢气加成的产物,则A的名称为:______;
②若A是炔烃与氢气加成的产物,则A的结构简式为:____。
(2)某烃B 0.1 mol 在氧气中充分燃烧后,可以生成7.2gH2O。试回答下列问题:
①若烃B不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯取代物有两种,则烃B的结构简式为_____。
②若烃B不能使溴水褪色,但能使酸性高锰酸钾溶液褪色,则烃B的可能的结构简式为_______
③若烃B能使溴水褪色,在催化剂作用下,与H2加成,其加成产物经测定分子中含有3个甲基,则烃B可能的结构简式_____。
(3)某烃C的相对分子质量为84。回答下列问题:
①下列物质与C以任意比例混合,若总物质的量一定,充分燃烧消耗氧气的量不相等的是(填序号)___。
a.C7H12O2 b.C6H14 c.C6H14O d.C7H14O3
②若烃C为链烃,与HBr加成后只能得到一种产物,且该烃的一氯代物只有一种。C的结构简式为________;名称是_____;在一定条件下能发生加聚反应,写出该反应的化学方程式_____ 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com