
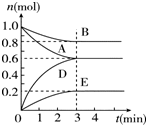
 T℃、2L密闭容器中某一反应在不同时刻的各物质的量如图所示(E为固体,其余为气体).回答下列问题.
T℃、2L密闭容器中某一反应在不同时刻的各物质的量如图所示(E为固体,其余为气体).回答下列问题.分析 (1)根据图象中各物质的物质的量变化确定其计量数之比,然后写出反应得到化学方程式;
(2)根据反应速率v=$\frac{△c}{△t}$计算出反应开始至3min时用D表示的平均反应速率;
(3)D为固体,该反应前后气体总体积相等,则压强不影响化学平衡,所以达到平衡时D的体积分数与原平衡相等.
解答 解:(1)根据图象曲线变化可知,A、B为反应物,C、D为生成物,A的物质的量变化为:1.0mol-0.6mol=0.4mol,B的物质的量变化为:1.0mol-0.8mol=0.2mol,D的物质的量变化为0.6mol,D的物质的量变化为0.2mol,根据物质的量变化与化学计量数成正比可知,A、B、D、E的计量数之比为=0.4mol:0.2mol:0.6mol:0.2mol=2:1:3:1,所以该反应的化学方程式为:2A(g)+B(g)?3D(g)+E(s),
故答案为:2A(g)+B(g)?3D(g)+E(s);
(2)反应开始至3min时,D的物质的量变化为0.6mol,则用D表示的平均反应速率为:v(D)=$\frac{\frac{0.6mol}{2L}}{3min}$=0.1mol•L-1•min-1,
故答案为:0.1;
(3)反应2A(g)+B(g)?3D(g)+E(s)中,反应前后气体的总物质的量不变,则压强不影响平衡,所以第6min时保持温度不变,将容器的体积缩小至原来的一半,重新达到平衡后,D的体积分数与原平衡相等,所以D的体积分数为:$\frac{0.6mo}{1mol+1mol}$×100%=30%,
故答案为:30%.
点评 本题考查了化学平衡的计算,题目难度中等,明确化学反应速率与化学计量数的关系为解答关键,注意该反应中D为固态,为易错点,试题培养了学生的分析能力及化学计算能力.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 该化合物仅含碳、氢两种元素 | B. | 该化合物中碳、氢原子个数比为1:8 | ||
| C. | 无法确定该化合物是否含有氧元素 | D. | 该化合物中一定含有氧元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向CuSO4溶液中加入Na2O2:2Na2O2+2Cu2++2H2O═4Na++2Cu(OH)2↓+O2↑ | |
| B. | 向Na2SiO3溶液中通入过量CO2:SiO32-+CO2+H2O═H2SiO3↓+CO32- | |
| C. | 向Al2(SO4)3溶液中加入过量NH3•H2O:Al3++4NH3•H2O═[Al(OH)4]-+4NH4+ | |
| D. | 向稀HNO3中滴加Na2SO3溶液:SO32-+2H+═SO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解稀硫酸溶液,实质上是电解水,故溶液pH不变 | |
| B. | 电解稀氢氧化钠溶液,要消耗OH-,故溶液pH减小 | |
| C. | 电解硫酸铜溶液,在阴极上和阳极上析出产物的物质的量之比为1:2 | |
| D. | 电解氯化铜溶液,消耗完氯化铜后电解就会停止 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | X的最高正价比Y的小 | |
| B. | X的最高价氧化物一定是X2O,Y的气态氢化物为H2Y | |
| C. | X的离子半径比Y的大 | |
| D. | X的核电荷数比Y的小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com