
 元素A的单质及元素A与元素B形成的化合物有如图所示的转化关系:
元素A的单质及元素A与元素B形成的化合物有如图所示的转化关系:
| ||
| ||


科目:高中化学 来源: 题型:
| A、34 g H2O2中含有的阴离子数为NA |
| B、在含Al3+总数为NA的AlCl3溶液中,Cl-总数为3NA |
| C、1mol重甲基(-CD3)含有电子数为9NA |
| D、1 mol铁铝混合物与足量稀盐酸反应时,转移电子数是3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
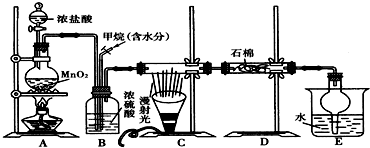
查看答案和解析>>
科目:高中化学 来源: 题型:
| 族 周期 | ||||||||
| 1 | ① | |||||||
| 2 | ② | |||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ||||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0族 |
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
| 4 | ⑨ | ⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 )在催化剂作用下发生缩聚反应生成聚乳酸:
)在催化剂作用下发生缩聚反应生成聚乳酸:查看答案和解析>>
科目:高中化学 来源: 题型:
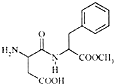 阿斯巴甜(Aspartame,结构简式如图)具有清爽的甜味,甜度约为蔗糖的200倍.下列有关说法不正确的是( )
阿斯巴甜(Aspartame,结构简式如图)具有清爽的甜味,甜度约为蔗糖的200倍.下列有关说法不正确的是( )| A、分子式为:C14H18N2O5,阿斯巴甜属于蛋白质 |
| B、阿斯巴甜能与H2发生加成反应 |
| C、阿斯巴甜在一定条件下既能与酸反应、又能与碱反应 |
| D、阿斯巴甜在一定条件下能发生水解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com