
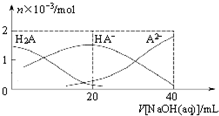
 25℃下,向20mL 0.1mol•L-1H2A溶液中滴加0.1mol•L-1NaOH溶液,有关粒子物质的量的变化如图所示.下列有关说法正确的是( )
25℃下,向20mL 0.1mol•L-1H2A溶液中滴加0.1mol•L-1NaOH溶液,有关粒子物质的量的变化如图所示.下列有关说法正确的是( )| A. | H2A属于强酸 | |
| B. | $\frac{c(H{A}^{-})}{c({H}_{2}{A}^{\;})}$随着V[NaOH(aq)]的增大而减小 | |
| C. | V[NaOH(aq)]=20mL时,溶液中存在关系:c(HA-)+c(A2-)+c(H2A)=0.1mol•L-1 | |
| D. | V[NaOH(aq)]=20mL时,溶液中存在关系:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-) |
分析 A.未加NaOH溶液时,溶液的pH在1-2之间,如果是强酸,溶液的pH=-lg0.2=0.7;
B.$\frac{c(H{A}^{-})}{c({H}_{2}{A}^{\;})}$随着V[NaOH(aq)]的增大先增大后减小;
C.任何电解质溶液中都存在物料守恒,根据物料守恒判断;
D.V[NaOH(aq)]=20mL时,二者恰好反应生成NaHA,根据图知,溶液中c(A2-)>c(H2A),说明HA-电离程度大于水解程度而导致溶液呈酸性.
解答 解:A.未加NaOH溶液时,如果是强酸,溶液的pH=-lg0.2=0.7,实际上溶液的pH在1-2之间,说明该酸部分电离,为弱电解质,故A错误;
B.根据图知,HA-先增大后减小,$\frac{c(H{A}^{-})}{c({H}_{2}{A}^{\;})}$随着V[NaOH(aq)]的增大先增大后减小,故B错误;
C.任何电解质溶液中都存在物料守恒,体积增大一倍,溶液中物质浓度降为原来的一半,根据物料守恒c(HA-)+c(A2-)+c(H2A)=0.05mol•L-1,故C错误;
D.V[NaOH(aq)]=20mL时,二者恰好反应生成NaHA,根据图知,溶液中c(A2-)>c(H2A),说明HA-电离程度大于水解程度而导致溶液呈酸性,但其水解和电离程度都较小,所以离子浓度大小顺序是c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-),故D正确;
故选D.
点评 本题考查酸碱混合溶液定性判断,为高频考点,正确分析图象是解本题关键,明确各点溶液中的溶质及其性质是解本题关键,易错选项是C,注意溶液体积增大一倍时其浓度降为原来一半.


 小题狂做系列答案
小题狂做系列答案科目:高中化学 来源: 题型:选择题
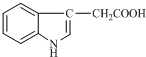 1934年,科学家首先从人尿中分离出具有生长素效应的化学物质--吲哚乙酸,吲哚乙酸的结构如图所示.下列有关吲哚乙酸的说法中正确的是( )
1934年,科学家首先从人尿中分离出具有生长素效应的化学物质--吲哚乙酸,吲哚乙酸的结构如图所示.下列有关吲哚乙酸的说法中正确的是( )| A. | 吲哚乙酸与苯丙氨酸互为同分异构体 | |
| B. | 吲哚乙酸可以发生取代反应、加成反应、氧化反应和还原反应 | |
| C. | 1mol吲哚乙酸与足量氢气发生加成反应时,可以消耗5mol H2 | |
| D. | 吲哚乙酸苯环上的二氯代物共有四种结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2+、Fe2+ | B. | Cu2+、Fe3+ | C. | Fe2+、Fe3+ | D. | Fe2+、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
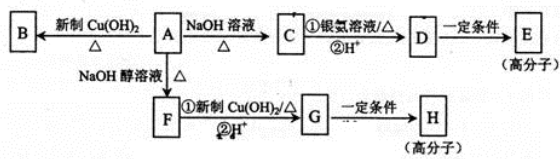
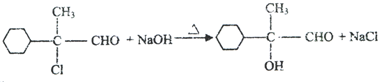 .
.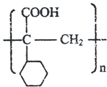 ,E的结构简式是
,E的结构简式是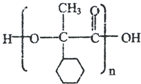 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
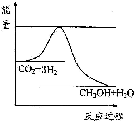 以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业叫煤化工.
以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业叫煤化工.| 起始 浓度 | 甲 | 乙 | 丙 |
| c(H2)/mol/L | 0.010 | 0.020 | 0.020 |
| c(CO2)/mol/L | 0.010 | 0.010 | 0.020 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
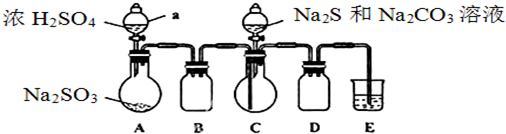
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com