
【题目】用下列装置(尾气处理已略去)进行相关实验,能实现实验目的的是

实验目的 | a中试剂 | b中试剂 | c中试剂 | |
A | 比较 | 醋酸溶液 | 碳酸钠 | 硅酸钠溶液 |
B | 比较 | 浓盐酸 | 高锰酸钾 | 碘化钾溶液 |
C | 证明苯和液溴发生取代反应 | 苯和液溴 | 铁粉 | 硝酸银溶液 |
D | 证明 | 饱和食盐水 | 电石 | 酸性高锰酸钾溶液 |
A. A B. B C. C D. D
 芝麻开花课程新体验系列答案
芝麻开花课程新体验系列答案科目:高中化学 来源: 题型:
【题目】已知化学反应A2(g)+B2(g)=2AB(g)△H=+100kJ/mol的能量变化如图所示,判断下列叙述中正确的是
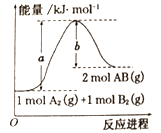
A. 加入催化剂,该反应的反应热△H将减小
B. 每生成2molA-B键,将吸收bkJ能量
C. 每生成2分子AB吸收(a-b)kJ能量
D. 该反应正反应的活化能大于100kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在1L恒容密闭容器中X,Y,Z三种气体的物质的量随时间变化曲线如图所示,以下说法正确的是( ) 
A.反应开始至2min,反应的平均速率v(Z)=0.2mol/L
B.该反应的化学方程式为X+3Y═2Z
C.该反应平衡时,Y转化率为30%
D.3min时,充入X,v正增大,v逆减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上通过2Al2O3+3C+6Cl2═4AlCl3+3CO2制取无水氯化铝,下列说法正确的是( )
A. AlCl3是氧化产物
B. Cl2是氧化剂
C. 每生成1 mol CO2,转移4个电子
D. C发生还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是( )
A.碳酸氢钠的热稳定性比碳酸钠的强
B.等质量的碳酸钠、碳酸氢钠分别与足量的盐酸反应,前者产生的二氧化碳多
C.足量的碳酸钠和碳酸氢钠分别与等物质的量的盐酸反应,两者产生的二氧化碳一样多
D.等物质的量的碳酸钠和碳酸氢钠分别与足量盐酸反应,前者消耗的盐酸多
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C、D、E五种微粒。已知:
①当A微粒失去3个电子后,其电子层结构与氖原子相同;
②当B微粒得到1个电子后其电子层结构与氩原子相同;
③C微粒带两个单位正电荷,核电荷数为12;
④D微粒有18个电子,当失去2个电子后显电中性;
⑤E微粒不带电,原子核中只有一个质子。
请回答:
(1)写出这五种微粒的符号:A_______,B_______,C_______,D______,E_______。
(2)B微粒的结构示意图________,D微粒的结构示意图_________。
(3)A的单质与EB溶液反应的离子方程式:_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知充分燃烧ag乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量bkJ,则乙炔燃烧的热化学方程式正确的是( )
A.2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣2bkJ/mol
B.C2H2(g)+ ![]() O2(g)═2CO2(g)+H2O(l)△H=2bkJ/mol
O2(g)═2CO2(g)+H2O(l)△H=2bkJ/mol
C.2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=﹣4bkJ/mol
D.2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=bkJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年IUPAC命名117号元素为Ts(中文名“ ![]() ”,tián),Ts的原子核外最外层电子数是7,下列说法不正确的是( )
”,tián),Ts的原子核外最外层电子数是7,下列说法不正确的是( )
A. Ts是第七周期第ⅦA族元素 B. Ts的同位素原子具有相同的电子数
C. Ts在同族元素中非金属性最弱 D. 中子数为176的TS核素符号是 ![]() Ts
Ts
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】表为周期表的一部分,其中的字母代表对应的元素,请针对这些元素回答下列问题. 
请回答下列问题:
(1)元素I的元素符号;已知M2+离子3d轨道中有6个电子,试推出M元素位于周期表的周期族.
(2)表中元素第一电离能最小的是(填元素符号,下同),电负性最大的是 , 化学性质最稳定的是 .
(3)表中元素处于d区的是(填元素符号).
(4)请举出F的金属性比C强的实验事实: , 并用原子结构理论解释其原因:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com