
 2SO3,△H<0.当气体的物质的量减少0.315mol时反应达到平衡,在相同温度下测得气体压强为反应前的82.5%.下列有关叙述正确的是( )
2SO3,△H<0.当气体的物质的量减少0.315mol时反应达到平衡,在相同温度下测得气体压强为反应前的82.5%.下列有关叙述正确的是( ) 2SO3可知,当气体的物质的量减少0.315mol时,生成SO30.63mol,以此计算;
2SO3可知,当气体的物质的量减少0.315mol时,生成SO30.63mol,以此计算; =82.5%,计算x可知SO2的物质的量为(x-1.1)mol,进而可计算转化率.
=82.5%,计算x可知SO2的物质的量为(x-1.1)mol,进而可计算转化率. 2SO3 △n
2SO3 △n =82.5%,x=1.8mol,
=82.5%,x=1.8mol, =90%,故D错误.
=90%,故D错误.

 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
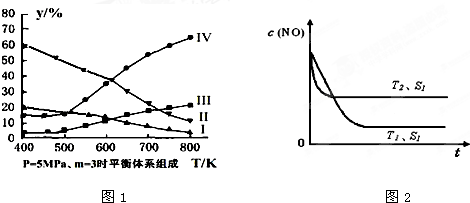
查看答案和解析>>
科目:高中化学 来源: 题型:
| 催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(2013?安徽模拟)已知反应2CH3OH(g)?CH3OCH3(g)+H2O(g)某温度下的平衡常数为400.此温度下,在体积恒定的密闭容器中加入一定量的CH3OH,反应到某时刻测得各组分的浓度如下:
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com