
| A、1.2g | B、2.2g |
| C、3.2g | D、无法计算 |
| 0.56L |
| 22.4L/mol |


科目:高中化学 来源: 题型:
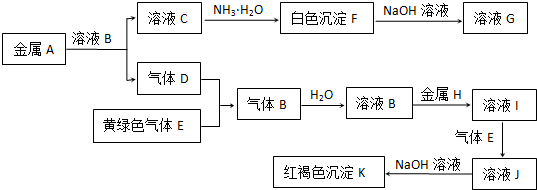
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、澄清透明溶液中:Cl-、NO3-、Cu2+、NH4+ |
| B、水电离产生的c(OH-)=1×10-11mol/L的溶液:Cu2+、SO42-、NO3-、Cl- |
| C、中性溶液中:Fe3+、Al3+、NO3-、SO42- |
| D、能使苯酚变紫色的溶液:K+、Mg2+、S2-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、等于98.32kJ |
| B、大于98.32kJ |
| C、小于98.32kJ |
| D、无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| ||
| △ |
| A、该反应是置换反应 |
| B、该反应是复分解反应 |
| C、碳元素化合价降低 |
| D、该反应是氧化还原反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com